Les codes de pratique existants concernant l’implication des patients avec les différentes parties prenantes ne couvrent pas l’ensemble du champ de la recherche et du développement (R&D). Depuis 2006, l’Agence européenne des médicaments (EMA) a mis en place un cadre complet d’interaction avec les patients et les organisations de consommateurs.
Les documents d’orientation de l’Académie européenne des patients (EUPATI) visent à soutenir l’intégration de la participation des patients dans l’ensemble du processus de recherche et de développement de médicaments avec les agences réglementaires, les organismes d’évaluation des technologies de la santé (ETS), les comités d’éthique et l’industrie pharmaceutique.
Les utilisateurs peuvent s’écarter des documents d’orientation en fonction de circonstances spécifiques, de la législation nationale ou des besoins propres à chaque interaction. Les documents d’orientation doivent être adaptés aux besoins individuels en faisant appel au meilleur jugement professionnel. Vous pouvez lire l’éditorial du guide ici.
EUPATI a publié quatre documents d’orientation détaillés sur l’implication des patients dans le domaine de la recherche et du développement (R&D). Ces documents couvrent des aspects clés, notamment les comités d’éthique, les organismes d’évaluation des technologies de la santé, les processus réglementaires et la recherche et le développement de médicaments menés par l’industrie pharmaceutique.
Chaque document d’orientation recommande des méthodes et des processus de travail et suggère des activités et des domaines spécifiques pour la participation des patients. Chaque document d’orientation propose des domaines clés offrant des possibilités d’implication des patients. Ils fournissent non seulement des recommandations pratiques sur la manière de faciliter des interactions efficaces et transparentes, mais aussi des indications précieuses sur les types de contribution des patients requis. Il peut s’agir de contributions individuelles tirées d’expériences anecdotiques de patients, de contributions de défenseurs des patients représentant des besoins plus larges des patients, de positions officielles défendues par des organisations de patients et de contributions de patients experts qui, en plus de leur savoir expérientiel, possèdent des compétences techniques et une formation.
Afin de garantir leur pertinence et leur alignement sur l’évolution des normes et de la législation, tous les documents d’orientation font l’objet d’un examen et d’une révision périodiques, reflétant la nature dynamique du domaine.
1. Orientations pour la participation des patients à la recherche et au développement de médicaments menés par l’industrie
Le document d’orientation de l’EUPATI présenté dans cet article vise à fournir des recommandations de règles de base et des propositions pour l’intégration de la participation des patients dans l’ensemble du processus de R&D des médicaments dans l’industrie pharmaceutique et décrit des activités spécifiques dans lesquelles les patients peuvent être impliqués et influencer la recherche et le développement futurs des médicaments.
2. Guide pour la participation des patients à l’ETS
Ce guide comprend un ensemble de « principes généraux » introductifs applicables tout au long du processus de recherche et de développement de médicaments ; la clause de non-responsabilité du guide ; le champ d’application du guide ; une explication de la définition du terme « patient » adoptée par l’EUPATI ; la raison d’être de l’élaboration du guide ; des informations générales sur la participation des patients à l’ETS en Europe ; et les objectifs finaux du guide. Ces sections sont suivies des recommandations (pratiques de travail et activités de participation des patients suggérées).
3. Orientations relatives à la participation des patients aux processus réglementaires
Les orientations d’EUPATI présentées dans cet article portent sur la participation des patients dans le domaine réglementaire. Il s’adresse principalement aux autorités réglementaires qui souhaitent interagir avec les patients ou leurs organisations dans le cadre de leurs activités, mais il devrait également être pris en compte par les patients et les organisations de patients qui envisagent de collaborer avec les autorités réglementaires.
4. Guide pour la participation des patients à l’évaluation éthique des essais cliniques
Ces lignes directrices ont été élaborées par l’Académie européenne des patients pour l’innovation thérapeutique (EUPATI) à l’intention de tous les acteurs du développement des médicaments qui participent à l’examen éthique des projets de recherche clinique, en particulier les membres des comités d’éthique de la recherche et les patients/soignants ou les représentants des patients qui apportent la contribution des patients.
Ces documents d’orientation jettent des bases solides pour l’implication des patients dans les processus complexes de la recherche et du développement de médicaments, en proposant des recommandations et des idées pratiques. La feuille de route pour l’implication des patients qui suit vise à donner aux parties prenantes les moyens de naviguer efficacement dans ces processus, en offrant un cadre systématique pour l’implication des patients tout au long du cycle de vie de la recherche et du développement.
Feuille de route pour l’engagement des patients
Vidéo de la feuille de route EUPATI sur l’implication des patients dans la R&D des médicaments
Qu’est-ce que la feuille de route EUPATI sur l’implication des patients ?
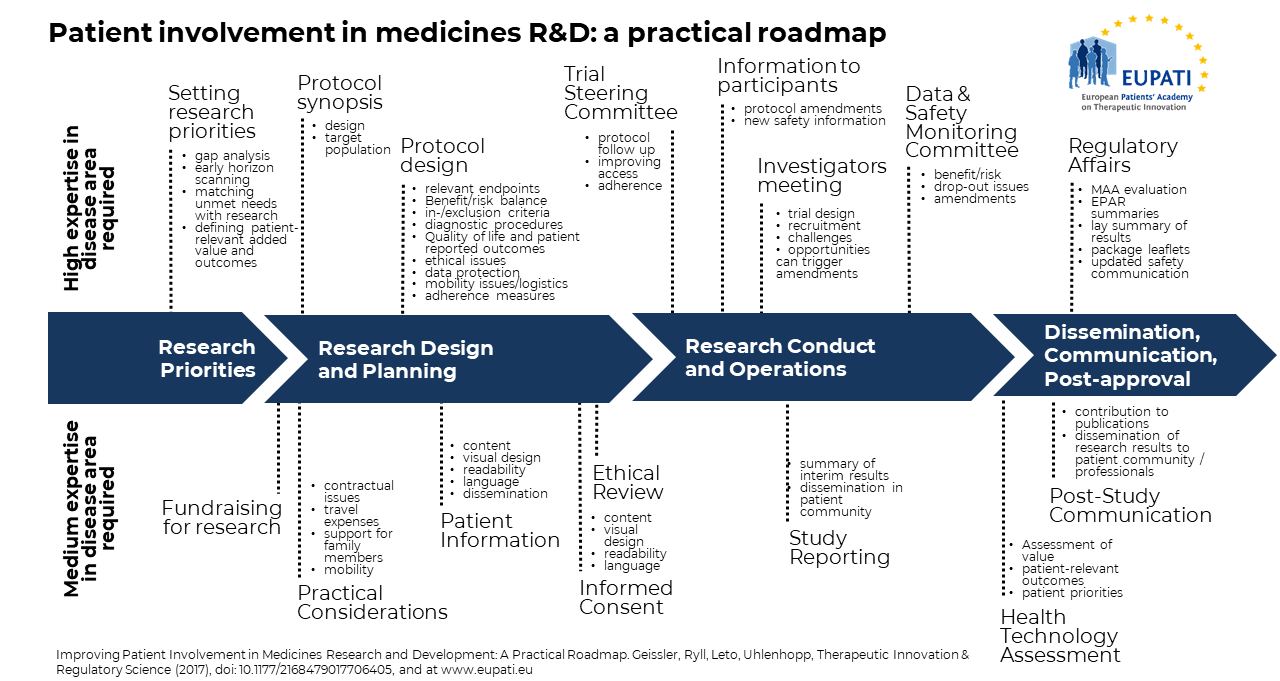
La valeur de l’implication des patients dans la recherche et le développement de médicaments est de plus en plus reconnue par toutes les parties prenantes. Malheureusement, la documentation formelle limitée des activités d’implication des patients entrave le partage des expériences et des enseignements, empêchant une mise en œuvre opportune et systématique. La participation des patients manque souvent de structure et de cohérence dans l’approche et arrive trop tard. Une ligne directrice pratique de bout en bout est nécessaire et la feuille de route EUPATI sur l’implication des patients, un modèle de processus pour l’implication des patients dans la recherche et le développement de médicaments, y pourvoit. Voir l’image ci-dessus (Source: Geissler, J., Ryll, B., Leto di Priolo, S., Uhlenhopp, M.: Improving Patient Involvement in Medicines Research and Development: A Practical Roadmap. Therapeutic Innovation & Regulatory Science 2017).
Utiliser la feuille de route EUPATI sur l’implication des patients
La feuille de route met en évidence les possibilités spécifiques d’implication des patients au cours des quatre étapes clés du cycle de vie de la recherche et du développement de médicaments et est illustrée par des exemples concrets. L’objectif de cette feuille de route est de fournir un outil pour faciliter l’implication des patients au cours de ce cycle de vie et elle est partagée afin d’encourager la mise en œuvre et le perfectionnement. La feuille de route a pour but de stimuler la discussion. Toutes les parties concernées, le monde universitaire et l’industrie pharmaceutique, les associations de patients et les patients, les cliniciens et les chercheurs, devront participer à l’identification des points stratégiques d’implication des patients et à leur mise en œuvre afin de maximiser les avantages pour toutes les parties prenantes.
L’engagement d’EUPATI dans la mise en œuvre de la feuille de route
La question d’une mise en œuvre réussie est un défi important, car la feuille de route et les documents d’orientation doivent être mis en pratique par les différentes parties prenantes. L’implication des patients dans la recherche peut être extrêmement bénéfique pour le processus de développement des médicaments : en apportant leurs priorités et leurs points de vue, les patients peuvent contribuer à la mise au point de meilleurs traitements pour eux et pour les autres. Une plus grande implication des patients dans la R&D renforcera l’efficacité et la sécurité des nouveaux traitements et augmentera le soutien du public à la recherche médicale. Pour ce faire, il est essentiel que les patients aient une connaissance approfondie des processus et des méthodes par lesquels les médicaments sont développés et mis sur le marché, afin de comprendre où et comment ils peuvent avoir un impact significatif. Les objectifs à long terme d’EUPATI restent axés sur le développement d’un contenu rigoureux pour l’éducation des patients, le perfectionnement des compétences des experts en matière de défense des intérêts des patients et le renforcement d’un mouvement européen des patients. L’EUPATI élargit également son champ d’activités pour inclure des formations destinées à d’autres parties prenantes, par exemple des formations sur l’engagement des patients pour les professionnels travaillant dans l’industrie et les universités.
[Clause de non-responsabilité : La traduction affichée a été générée à l’aide d’un système de traitement automatique des langues.]