I codici di condotta esistenti per il coinvolgimento dei pazienti con le varie parti interessate non coprono in modo esaustivo l’intero ambito della ricerca e sviluppo (R&S). Dal 2006 l’Agenzia Europea dei Medicinali (EMA) ha sviluppato un quadro completo di interazione con i pazienti e le organizzazioni dei consumatori.
I documenti di orientamento dell’Accademia Europea dei Pazienti (EUPATI) mirano a sostenere l’integrazione del coinvolgimento dei pazienti nell’intero processo di ricerca e sviluppo dei farmaci con le agenzie regolatorie, gli organismi di valutazione delle tecnologie sanitarie (HTA), i comitati etici e l’industria farmaceutica.
Gli utenti possono discostarsi dalle linee guida in base a circostanze specifiche, alla legislazione nazionale o alle esigenze uniche di ciascuna interazione. I documenti di orientamento devono essere adattati alle esigenze individuali utilizzando il miglior giudizio professionale. È possibile leggere l’editoriale della guida qui.
EUPATI ha pubblicato quattro documenti guida completi che trattano il coinvolgimento dei pazienti nel campo della ricerca e sviluppo (R&S). Questi documenti coprono aspetti chiave, tra cui i comitati etici, gli organismi di valutazione delle tecnologie sanitarie, i processi normativi e la R&S sui farmaci guidata dall’industria farmaceutica.
Ogni documento guida raccomanda metodi e processi di lavoro e suggerisce attività e aree specifiche per il coinvolgimento dei pazienti. Ogni Guida suggerisce aree chiave con opportunità di coinvolgimento dei pazienti. Non solo forniscono raccomandazioni pratiche su come facilitare interazioni efficaci e trasparenti, ma offrono anche indicazioni preziose sul tipo di contributo richiesto dai pazienti. Si tratta di contributi individuali tratti da esperienze aneddotiche dei pazienti, di contributi di sostenitori dei pazienti che rappresentano le esigenze più ampie dei pazienti, di posizioni formali sostenute da organizzazioni di pazienti e di contributi di esperti di pazienti che, oltre alle loro conoscenze esperienziali, possiedono competenze tecniche e formazione.
Per garantirne la pertinenza e l’allineamento con l’evoluzione degli standard e della legislazione, tutti i documenti guida sono sottoposti a revisioni periodiche, che riflettono la natura dinamica del settore.
1. Linee guida per il coinvolgimento dei pazienti nelle attività di R&S sui farmaci condotte dall’industria
Il documento di orientamento EUPATI in questo articolo mira a fornire raccomandazioni per le regole di base e proposte per l’integrazione del coinvolgimento dei pazienti nell’intero processo di R&S dei farmaci nell’industria farmaceutica e delinea attività specifiche in cui i pazienti possono essere coinvolti e influenzare la ricerca e lo sviluppo dei farmaci futuri.
2. Linee guida per il coinvolgimento dei pazienti nell’HTA
La presente Guida comprende una serie di “principi generali” introduttivi applicabili all’intero processo di ricerca e sviluppo dei farmaci; il disclaimer della Guida; l’ambito di applicazione della Guida; una spiegazione della definizione del termine “paziente” adottata da EUPATI; le motivazioni per lo sviluppo della Guida; informazioni di base sul coinvolgimento dei pazienti nell’HTA in Europa; gli obiettivi finali della Guida. Queste sezioni sono seguite dalle raccomandazioni (pratiche di lavoro suggerite e attività di coinvolgimento dei pazienti).
3. Linee guida per il coinvolgimento dei pazienti nei processi regolatori
La Guida EUPATI di questo articolo riguarda il coinvolgimento dei pazienti in ambito regolatorio. È rivolta principalmente alle autorità regolatorie che desiderano interagire con i pazienti o le loro organizzazioni nelle loro attività, ma dovrebbe essere presa in considerazione anche da pazienti/organizzazioni di pazienti che intendono collaborare con le autorità regolatorie.
4. Linee guida per il coinvolgimento dei pazienti nella revisione etica delle sperimentazioni cliniche
Queste linee guida sono state sviluppate dalla European Patient Academy on Therapeutic Innovation (EUPATI) per tutte le parti interessate allo sviluppo dei farmaci coinvolte nella revisione etica dei progetti di ricerca clinica, con particolare attenzione ai membri dei comitati etici di ricerca e ai pazienti/curatori o rappresentanti dei pazienti che forniscono il loro contributo.
Questi documenti di orientamento pongono una solida base per il coinvolgimento dei pazienti negli intricati processi di R&S dei farmaci, garantendo raccomandazioni e approfondimenti pratici, mentre la seguente Patient Engagement Roadmap mira a mettere ulteriormente in grado gli stakeholder di navigare in questi processi in modo efficiente, offrendo un quadro sistematico per il coinvolgimento dei pazienti durante l’intero ciclo di vita della R&S.
Tabella di marcia per il coinvolgimento dei pazienti
La roadmap EUPATI per il coinvolgimento dei pazienti nella R&S dei medicinali Video
Cos’è la roadmap EUPATI sul coinvolgimento dei pazienti?
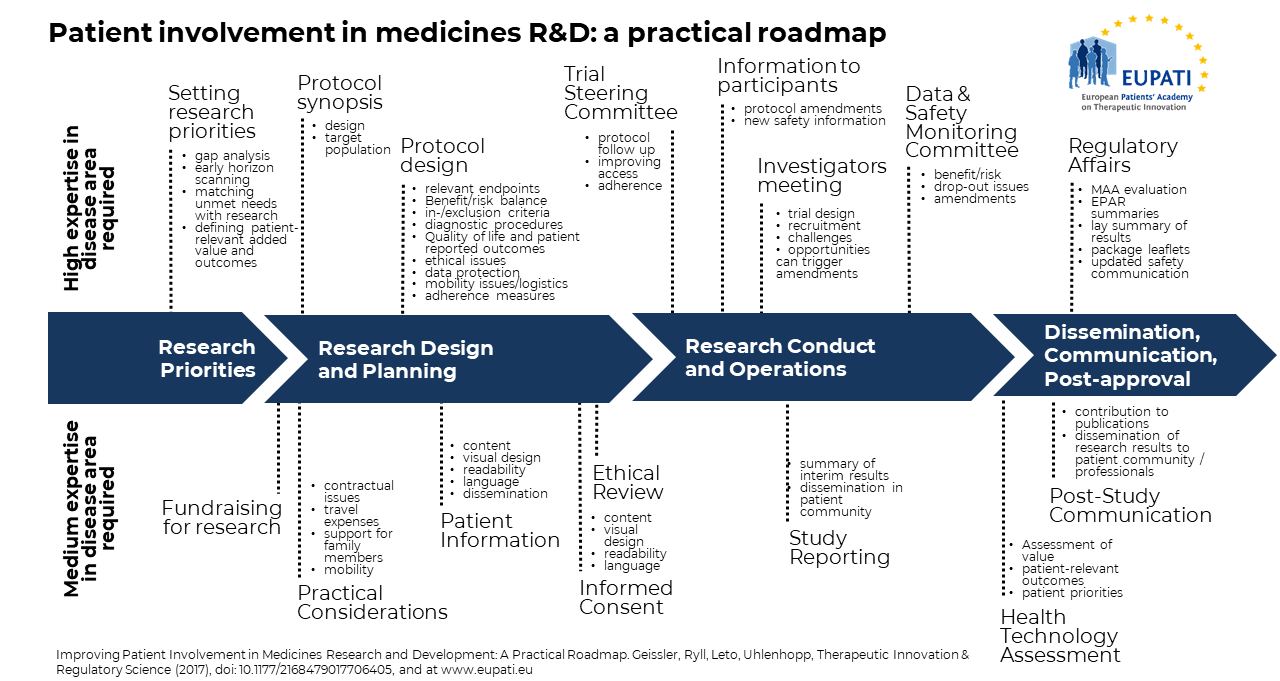
Il valore del coinvolgimento dei pazienti nella ricerca e nello sviluppo dei farmaci è sempre più riconosciuto da tutte le parti interessate. Purtroppo, una limitata documentazione formale delle attività di coinvolgimento dei pazienti ostacola la condivisione delle esperienze e degli apprendimenti, impedendo un’implementazione tempestiva e sistematica. Il coinvolgimento dei pazienti spesso manca di struttura e coerenza nell’approccio e avviene troppo tardi. È necessaria una linea guida pratica e completa, che EUPATI fornisce con la sua Patient Engagement Roadmap, un modello di processo per il coinvolgimento dei pazienti nella ricerca e nello sviluppo dei farmaci. Si veda l’immagine qui sopra (Fonte: Geissler, J., Ryll, B., Leto di Priolo, S., Uhlenhopp, M.: Improving Patient Involvement in Medicines Research and Development: A Practical Roadmap. Therapeutic Innovation & Regulatory Science 2017).
Utilizzo della tabella di marcia per il coinvolgimento dei pazienti di EUPATI
La roadmap evidenzia opportunità specifiche per il coinvolgimento dei pazienti lungo le quattro fasi chiave del ciclo di vita della ricerca e dello sviluppo dei farmaci ed è illustrata con esempi concreti. L’obiettivo di questa roadmap è fornire uno strumento per facilitare il coinvolgimento dei pazienti durante questo ciclo di vita e viene condivisa per incoraggiare l’implementazione e l’ulteriore perfezionamento. La roadmap intende stimolare ulteriori discussioni. Tutte le parti coinvolte, il mondo accademico e l’industria farmaceutica, le organizzazioni di pazienti e i pazienti, i clinici e i ricercatori, dovranno essere coinvolti nell’identificazione dei punti strategici di coinvolgimento dei pazienti e nella loro attuazione per massimizzare i benefici per tutte le parti interessate.
L’impegno di EUPATI nell’attuazione della Roadmap
La questione del successo dell’implementazione è una sfida importante, poiché la Roadmap e i documenti guida devono essere messi in pratica dai diversi stakeholder. Il coinvolgimento dei pazienti nella ricerca può portare enormi benefici al processo di sviluppo dei farmaci: apportando le loro priorità e prospettive, i pazienti possono contribuire allo sviluppo di trattamenti migliori per loro e per gli altri. Un maggiore coinvolgimento dei pazienti nella R&S aumenterà l’efficacia e la sicurezza dei nuovi trattamenti e aumenterà il sostegno pubblico alla ricerca medica. A tal fine, è essenziale che i pazienti abbiano una conoscenza approfondita dei processi e dei metodi con cui i farmaci vengono sviluppati e immessi sul mercato, per capire dove e come possono avere un impatto significativo. Gli obiettivi a lungo termine di EUPATI rimangono incentrati sullo sviluppo di contenuti rigorosi per l’educazione dei pazienti, sul miglioramento delle capacità di advocacy degli esperti dei pazienti e sul rafforzamento di un movimento europeo di pazienti. EUPATI sta inoltre ampliando la portata delle sue attività per includere la formazione di altri stakeholder, ad esempio la formazione sul coinvolgimento dei pazienti per i professionisti che lavorano nell’industria e nel mondo accademico.
[Esclusione di responsabilità: la traduzione visualizzata è stata generata con un sistema di elaborazione automatica del linguaggio.]