Last update: 23 Novembre 2015
Introduzione
Questo articolo si concentra sulla legislazione dell’Unione Europea (UE) e sulle linee guida dell’Agenzia europea per i medicinali (EMA). Non considera in dettaglio la legislazione nazionale o linee guida al di fuori della UE. I ruoli di organizzazioni di pazienti sono descritti a livello dell’EMA.
L’Agenzia europea per i medicinali (EMA)
L’Agenzia europea per i medicinali (EMA) è responsabile per la valutazione scientifica di prodotti medicinali per uso umano e veterinario nell’Unione Europea.
Dalla sua fondazione nel 1995 l’EMA è impegnata nel dialogo tra pazienti e consumatori europei. In veste di utenti dei medicinali valutati dalla EMA, i pazienti sono al centro del lavoro dell’EMA come principali parti interessate e offrono conoscenze ed esperienze specifiche.
I pazienti e i consumatori sono coinvolti in numerose attività alla EMA che vanno dalla revisione di informazioni preparate dall’EMA su medicinali, al coinvolgimento nella preparazione di linee guida, dalla partecipazione a gruppi di consulenza scientifica e al ruolo di membro nei comitati scientifici dell’EMA.
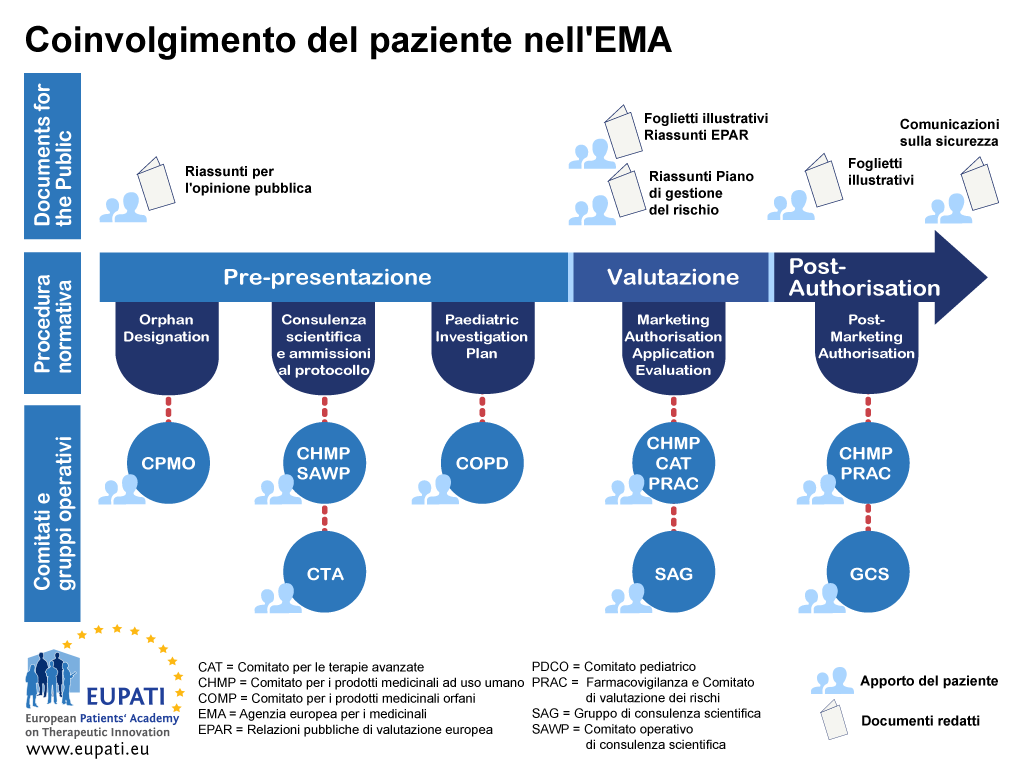
Coinvolgimento del paziente nei Comitati normativi dell’EMA
Ad oggi l’implementazione di una legislazione comunitaria ha portato alla partecipazione in veste di membri di pazienti in quattro dei comitati scientifici dell’EMA: il Comitato per i prodotti medicinali orfani (COMP), il Comitato pediatrico (PDCO), il Comitato per le terapie avanzate (CAT) e il Comitato di valutazione dei rischi per la farmacovigilanza (PRAC). I pazienti sono rappresentati anche nel Comitato di gestione EMA.
Comitato per i prodotti medicinali orfani (COMP)
Dalla sua prima riunione nell'aprile del 2000 il COMP comprende tra i suoi membri tre membri nominati dalle organizzazioni di rappresentanza dei pazienti della Commissione Europea con nomina rinnovabile di tre anni.
Comitato pediatrico (PDCO)
Dal settembre 2008 il PDCO comprende tra i suoi membri tre membri e tre sostituti nominati dalle associazioni di rappresentanza dei pazienti della Commissione Europea con nomina rinnovabile di tre anni.
Comitato per le terapie avanzate (CAT)
Dal gennaio 2009 il CAT comprende tra i suoi membri due membri e due sostituti nominati dalle associazioni di rappresentanza dei pazienti della Commissione Europea con nomina rinnovabile di tre anni.
Comitato di valutazione dei rischi per la farmacovigilanza (PRAC)
Dal luglio 2012 il PRAC comprende tra i suoi membri un membro e un sostituto nominati dalle associazioni di rappresentanza dei pazienti della Commissione Europea con nomina rinnovabile di tre anni.
Il ruolo e il valore dei pazienti come membri dei comitati scientifici
I pazienti che sono membri dei comitati scientifici EMA hanno lo stesso ruolo di tutti gli altri membri. L'esperienza ha dimostrato che i pazienti danno spesso un contributo scientifico alla discussione. Avere pazienti e consumatori nei comitati scientifici è un valore aggiunto che si traduce in un input esclusivo e fondamentale basato sulla loro esperienza di vita reale derivante dal fatto che sono affetti da una malattia e dal loro ambiente terapeutico attuale. Gli sforzi dei pazienti dovrebbero concentrarsi sull'assicurazione di questa prospettiva esclusiva estesa a tutte le attività del comitato e a tutti i risultati.
Tutti i membri del comitato:
- Partecipano in conformità con le norme di procedura del comitato e i compiti definiti
- Mantengono la riservatezza, rendono noto ogni conflitto d'interesse, e si attengono al codice di comportamento dell'EMA
- Partecipano alle decisioni del comitato e hanno lo stesso potere di voto. I sostituti possono partecipare a tutte le riunioni del comitato e contribuiscono al lavoro e alle discussioni all'interno del comitato con pari diritti.
Ulteriori risorse
- Agenzia europea per i medicinali (2014). EMA/652164/2014 Allegato II: Le attività dell'EMA in cui sono coinvolti pazienti* e consumatori. Scaricato il 31 agosto 2015, da http://www.ema.europa.eu/docs/en_GB/document_library/Other/2014/12/WC500179568.pdf
- Agenzia europea per i medicinali (2014). EMA/24913/2005 – rev. 2. Criteri che devono essere soddisfati dalle organizzazioni di pazienti e consumatori che partecipano alle attività dell'Agenzia europea per i medicinali (EMA). Scaricato il 4 settembre 2015 da http://www.ema.europa.eu/docs/en_GB/document_library/Regulatory_and_procedural_guideline/2009/12/WC500018099.pdf
- Agenzia europea per i medicinali (2013). EMA/272219/2013 Sesto rapporto annuale sull'interazione con le organizzazioni di pazienti e consumatori (2012). Scaricato il 4 settembre 2015 da http://www.ema.europa.eu/docs/en_GB/document_library/Regulatory_and_procedural_guideline/2009/12/WC500018099.pdf
Allegati
A2-5.08.1-v1.3