Last update: 23 listopada 2015
Wprowadzenie
Ocena technologii medycznych (Health Technology Assessment, HTA) to rodzaj badań pozwalających uzyskać informacje o klinicznych i ekonomicznych aspektach technologii medycznych.
W opiece zdrowotnej termin technologia medyczna (lub w skrócie technologia) może dotyczyć produktów leczniczych (leki, także biologiczne), urządzeń medycznych, sprzętu i materiałów eksploatacyjnych; procedur medycznych i chirurgicznych; programów zdrowia publicznego i systemów wsparcia oraz systemów organizacji i zarządzania stosowanych w profilaktyce, badaniach przesiewowych, diagnozowaniu, leczeniu i rehabilitacji.
Są to na przykład:
- Leki
- Programy zapobiegające złym stanom zdrowia (np. programy szczepień dzieci)
- Procedury (takie jak zabiegi chirurgiczne)
- Urządzenia (sprzęt lub maszyny stosowane do interwencji medycznych lub do codziennej pomocy, takie jak pompa insulinowa lub automatyczny wstrzykiwacz epinefryny)
Co wchodzi w zakres oceny HTA?
Ocena technologii medycznych (Health Technology Assessment, HTA) to systematyczne badanie właściwości, efektów i/lub wpływu technologii medycznych. Może dotyczyć zarówno bezpośrednich i zamierzonych, jak i pośrednich i niezamierzonych konsekwencji stosowania technologii.
Głównym celem oceny HTA jest informowanie osób związanych z technologią, odpowiedzialnych za politykę opieki zdrowotnej. Czasem oceny HTA określane są jako „łącznik między dowodami i tworzeniem polityki”. Oceny HTA są przeprowadzane przez interdyscyplinarne grupy za pomocą analitycznych struktur pochodzących z różnych metod. Ponieważ organy i procesy HTA w różnych krajach, a niekiedy regionach, są odmienne, nie ma wspólnej (zharmonizowanej) metody przeprowadzania oceny HTA. Jednak w ostatnich latach dokonała się większa standaryzacja podstaw dobrych procesów HTA.
Integracja organizacyjna organów HTA z systemem opieki zdrowotnej jest różna i zależy od kraju.
Odpowiedzialność
Organ HTA musi mieć określony zakres odpowiedzialności, który wyznacza, jakie technologie będą lub nie będą oceniane. Zakres odpowiedzialności organu HTA wpływa także na wiele innych aspektów procesu HTA, w tym na interakcje organu HTA z organizacjami innymi niż decyzyjne, na możliwy do realizacji lub wymagany poziom przejrzystości oraz na zaangażowanie w proces osób z zewnątrz. Miejsce organu HTA w systemie opieki zdrowotnej odgrywa kluczową rolę w wyznaczeniu jego zakresu odpowiedzialności. Organy HTA mogą istnieć w różnych organizacjach — mogą na przykład wchodzić w skład ministerstwa zdrowia, rady ds. jakości lub uniwersytetu, a mogą także być samodzielną jednostką upoważnioną prawnie do działania. Aby organy HTA były skuteczne, powinny mieć połączenie z decydentami.
Procesy i metody
Zakres, wybór metod i poziom szczegółowości działań HTA są bardzo różne. W skróconej formie HTA można scharakteryzować za pomocą trzech faz:
- Ocena: zestawienie i krytyczny przegląd dowodów naukowych
- Weryfikacja: przegląd oceny z uwzględnieniem wszystkich innych (politycznych) czynników przeprowadzany przez komisję w celu udzielenia rekomendacji
- Podejmowanie decyzji: wdrożenie rekomendacji
Każda z tych trzech faz składa się z różnych struktur i funkcji. Nie wszystkie programy HTA wymagają przeprowadzenia wszystkich powyższych etapów, w rzeczywistości „podejmowanie decyzji” rzadko, jeśli w ogóle, jest obowiązkiem organu HTA.
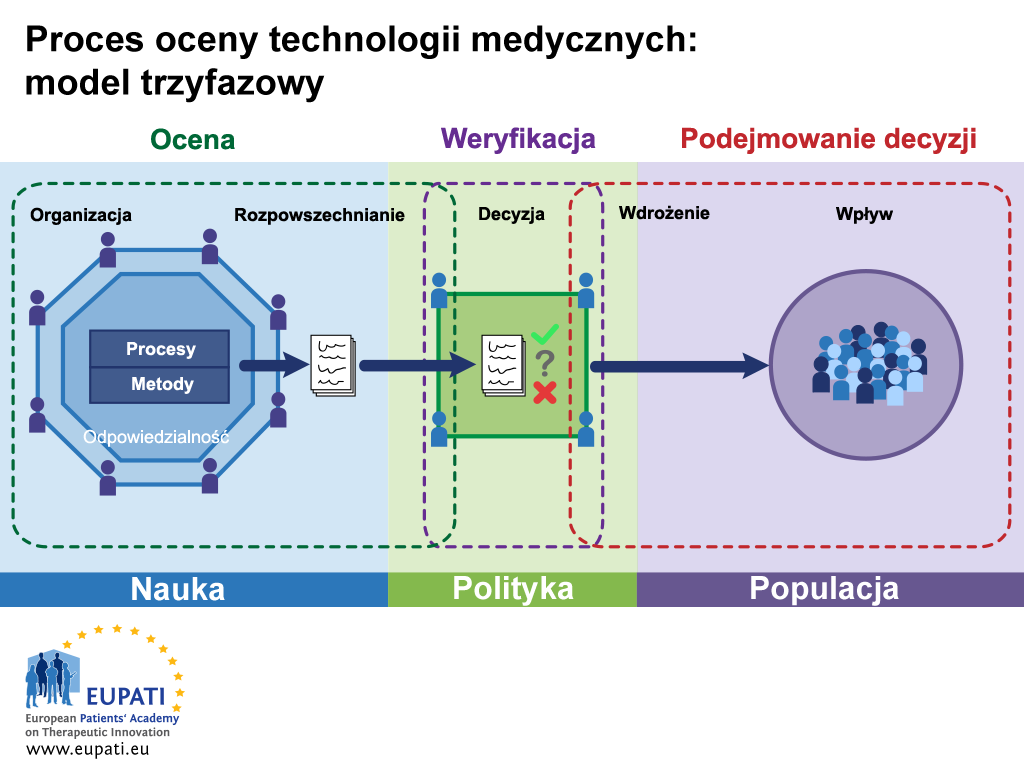
Rys. 1 przedstawia ogólny (uproszczony) proces HTA. Podkreśla cel procesu HTA: przekazywanie informacji z badań medycznych (nauka) decydentom, a ostatecznie populacji.
- Uproszczony model oceny technologii medycznych pokazuje interakcje między trzema fazami w nauce, polityce i populacji.
Organy HTA muszą decydować, jakie informacje na temat technologii będą ważne dla decydentów i jak te informacje zostaną zebrane. Podejmowane przez organ HTA decyzje dotyczące stosowanych procesów i metod wpływają na oceny, a same podlegają wpływom organizacji i zakresowi odpowiedzialności organu HTA.
Organy HTA muszą określić, jaka wiedza o konsekwencjach i wpływie stosowania technologii medycznej jest ważna dla decydentów i w jakim zakresie ich oceny powinny być zawężane (do jednej technologii). Na przykład wiedza o klinicznej skuteczności technologii medycznej jest zwykle uważna za ważną dla decydentów, jednak ze stosowaniem niektórych technologii medycznych mogą się wiązać problemy etyczne, a inne mogą być od nich wolne. Organ HTA musi zdecydować, czy zastosuje jeden standardowy proces do wszystkich technologii medycznych, czy też umożliwi stosowanie specjalnych procesów do indywidualnej oceny każdej z nich na podstawie wymaganych informacji. W takim wypadku, czy informacje dotyczące etyki powinny być gromadzone dla wszystkich ocenianych technologii, czy też pojawi się oddzielny proces, dostarczający w razie potrzeby takich danych?
Większość ocen HTA obejmuje jakąś formę następujących podstawowych etapów:
- Identyfikacja ocenianych zagadnień
- Określenie problemów lub pytań związanych z oceną
- Pozyskanie odpowiedniego dostępnego dowodu
- Utworzenie lub pozyskanie nowego dowodu (co jest właściwe)
- Weryfikacja/interpretacja jakości dowodu
- Integracja/synteza dowodu
- Sformułowanie wniosków i rekomendacji
- Rozpowszechnienie wniosków i rekomendacji
- Monitorowanie wpływu
Nie wszystkie organy HTA przeprowadzają wszystkie te etapy i niekoniecznie robią to w kolejności.
Ocena
Metody i procesy stosowane przez organ HTA w fazie oceny są ważne w celu zapewnienia spójnej oceny nowych technologii medycznych. Jeśli organowi HTA nie uda się na przykład wystandaryzować metod stosowanych do prowadzenia przeglądu literatury lub syntezy informacji, może on niespójnie oceniać nowe technologie. HTA może stosować zróżnicowaną grupę metod.
Dwa zasadnicze typy metod HTA to metody gromadzenia danych głównych i metody dodatkowe lub integracyjne. Metody gromadzenia danych głównych obejmują zbieranie oryginalnych danych, na przykład z badań klinicznych i obserwacyjnych. Metody integracyjne lub dodatkowe, lub syntetyczne obejmują łączenie danych bądź informacji z istniejących źródeł, w tym z badań danych głównych. Metody analizy ekonomicznej mogą obejmować jedną lub obie metody danych głównych i metody integracyjne.
W celu sformułowania wniosków wiele organów HTA polega w większości na integracyjnych metodach sprawdzania i syntezy danych (za pomocą systematycznych przeglądów i metaanaliz na podstawie istniejących odpowiednich badań danych głównych (zgłaszanych w artykułach w magazynach lub uzyskiwanych z epidemiologicznych lub administracyjnych zestawów danych). Ich oceny opierają się na rozróżnieniu między silniejszymi i słabszymi dowodami pochodzącymi z dostępnych badań danych głównych.
Niektóre oceny obejmują wiele cykli pozyskiwania/gromadzenia, interpretowania i integrowania dowodów przez ostatecznym zakończeniem.
Nie zawsze jest możliwe przeprowadzenie lub oparcie oceny na najbardziej rygorystycznych typach badań. W rzeczywistości zasady często muszą być ustanawiane przy braku ostatecznych badań lub przed ich zakończeniem. Wziąwszy pod uwagę różne orientacje ocen, ograniczenia zasobów i inne czynniki, organy HTA zwykle polegają na połączeniu różnych metod.
Na przykład, aby ocenić technologię, organ HTA może wymagać dowodów rozwiązujących wiele problemów, a w tym:
- Obciążenie chorobą
- Prognozowane trendy epidemiologiczne choroby
- Względną skuteczność technologii
- Opłacalność technologii. (Należy pamiętać, że nie wszystkie organy HTA biorą pod uwagę opłacalność. Niektóre koncentrują się bardziej na korzyściach klinicznych i wpływie na budżet).
- To, jak pacjenci oceniają wyniki terapii.
W niektórych wypadkach organy HTA mogą odpowiadać na te pytania bezpośrednio lub podejmując nowe badania. W innych wypadkach mogą prosić producenta leku o dostarczenie odpowiednich informacji.
Rozpowszechnianie
Rozpowszechnianie wyników i rekomendacji oraz monitorowanie wpływu mogą, ale nie muszą wchodzić w skład działań związanych z oceną HTA, ale pozostają w gestii wyznaczonej organizacji.
W większości wypadków może być potrzebne wyjaśnienie raportu HTA osobom nieznającym szczegółów badań klinicznych ani ocen ekonomicznych. Zależnie od organizacji organu HTA i jego relacji z decydentami może być potrzebna publikacja raportu HTA w różnych formatach — takich jak druk, bezpośrednia prezentacja lub oba. Może też okazać się potrzebna fachowa recenzja. Sposób prezentowania informacji i poziom użytego języka technicznego może zależeć od tego, czy jest ona przeznaczona dla komisji ekspertów czy bezpośrednio dla decydentów.
Decyzja
Ostatecznym celem procesu HTA jest wspieranie decyzji w zakresie polityki zdrowotnej. Na tym etapie procesu zebrane i ocenione przez organ HTA informacje są weryfikowane przez decydentów (na przykład krajowe systemy opieki zdrowotnej, ubezpieczycieli itd.). Choć przyjmuje się, że są one podejmowane niezależnie od organu HTA, jednak sposób ich podejmowania wpływa na proces HTA. Na przykład, jeśli można złożyć sprzeciw wobec decyzji, w efekcie organ HTA może zostać poproszony o przeprowadzenie dalszych analiz. Jeśli decyzje są podejmowane przy udziale komisji eksperckiej, organ HTA może być zmuszony do koordynacji jego prac lub udziału w spotkaniach. Może istnieć wymaganie zapewnienia poufności raportów HTA lub umożliwienia ich publicznego komentowania.
Wdrożenie i wpływ
Jeśli decydenci podejmują decyzję na podstawie raportu HTA (rekomendacja), taka decyzja powinna zostać wdrożona w społeczeństwie, a w efekcie będzie wpływać na populację. W procesie weryfikacji przeprowadzanym przez organ HTA należy uwzględniać to, jak takie decyzje są wdrażane i jak rekomendacje HTA mogą wpływać na populację. Można także stworzyć metodę zbierania opinii, która pozwoli organowi HTA mierzyć wpływ na populację wydawanych rekomendacji , aby brać go pod uwagę na etapach podejmowania decyzji.
W poniższej Tabeli 1 przedstawiono różne etapy procesu HTA i pewne pytania, na które organizacja HTA powinna znaleźć odpowiedź aby opracować „dobry” proces HTA. Lista pytań nie jest wyczerpująca — zależnie od sytuacji organizacji i tego, kto ją wspiera, mogą pojawić się inne.
| Etap | Właściwe kwestie do rozważenia |
|---|---|
| Organizacja |
|
| Odpowiedzialność |
|
| Metody i procesy |
|
| Rozpowszechnianie |
|
| Decyzja |
|
| Wdrożenie |
|
| Wpływ |
|
Załącznik
- Arkusz informacyjny: Etapy procesów HTA i kwestie do rozważenia
Size: 113,171 bytes, Format: .docx
W tym arkuszu informacyjnym przedstawiono kolejne kwestie do rozpatrzenia na każdym z etapów procesu HTA.
A2-6.02.1-v1.1