Last update: 19 November 2015
Einleitung
Lisa leidet nach einem Eingriff unter starken Schmerzen. Der Arzt hat die Wahl zwischen Tabletten, für die die externe klinische Evidenz spricht, und einer Injektion, die seiner persönlichen klinischen Erfahrung nach besser geeignet ist und zudem von der Patientin bevorzugt wird. Er weiß, dass laut der externen klinischen Evidenz morphinhaltige Tabletten die beste Wahl darstellen. Das Anästhetikum, das Lisa bei dem operativen Eingriff verabreicht wurde, führt jedoch häufig zu Erbrechen. Das bedeutet: Wenn Lisa sich nach Einnahme einer Tablette übergibt, wird der in der Tablette enthaltene Wirkstoff nicht in den Körper gelangen und die schmerzlindernde Wirkung damit ausbleiben. Der Arzt und Lisa wissen aus Erfahrung, dass Lisa sich mit ziemlicher Wahrscheinlichkeit innerhalb von 30 Minuten nach Absetzen der Anästhesie erbrechen wird. Aus diesem Grund entscheidet sich der Arzt dafür, Lisa stattdessen eine morphinhaltige Injektion zu verabreichen.
In diesem Beispiel entscheidet der Arzt auf Grundlage seiner persönlichen klinischen Erfahrung und den Präferenzen der Patientin, statt der morphinhaltigen Tabletten, für die die beste externe klinische Evidenz vorliegt, eine Morphininjektion zu verabreichen. Der Arzt setzt denselben medizinischen Wirkstoff (Morphin) ein, der von der externen klinischen Evidenz empfohlen wird, wählt jedoch eine andere Formulierung (Injektion statt Tablette).
Dies ist ein Beispiel dafür, wie ein Arzt nach Besprechung der Behandlungsoptionen mit dem Patienten auf Grundlage der vorliegenden Evidenz zu einer bestimmten Behandlungsentscheidung gelangt.
Was ist „Evidenzbasierte Medizin“?
Evidenzbasierte Medizin (EBM) der Prozess der systematischen Durchsicht, Bewertung und Anwendung klinischer Forschungserkenntnisse mit dem Ziel der Bereitstellung einer optimalen klinischen Versorgung für Patienten. Es ist wichtig, dass Patienten von der evidenzbasierten Medizin wissen, da dieses Wissen es ihnen ermöglicht, fundierte Entscheidungen hinsichtlich des Umgangs mit und der Behandlung der Erkrankung zu treffen. Zudem ermöglicht es den Patienten eine zutreffendere Einschätzung des Risikos, fördert die angemessene Durchführung elektiver Maßnahmen, und unterstützt die evidenzbasierte Entscheidungsfindung durch Arzt und Patient.
Evidenzbasierte Medizin ist eine Kombination aus Prinzipien und Methoden. In die Tat umgesetzt stellen diese sicher, dass medizinische Entscheidungen, Leitlinien und Richtlinien auf der derzeit besten Evidenz hinsichtlich der Wirkung verschiedener Behandlungsformen und der Gesundheitspflege im Allgemeinen basieren. Bezogen auf Arzneimittel stützt sie sich stark auf Informationen aus der Evaluierung von Nutzen und Risiken (Wirksamkeit und Sicherheit).
Das Konzept der evidenzbasierten Medizin entstand in den 1950er Jahren. Davor basierten medizinische Entscheidungen in der Hauptsache auf der medizinischen Ausbildung, der klinischen Erfahrung und des durch die Lektüre von Fachzeitschriften erworbenen Wissens. Studien zeigten jedoch substantielle Abweichungen zwischen den von unterschiedlichen Ärzten in derselben Situation getroffenen medizinischen Behandlungsentscheidungen. Diese Erkenntnis bildete die Grundlage für die Implementierung systematischer Methoden für die Erfassung, Evaluierung und Gliederung von Forschungsdaten und damit letztlich für das Aufkommen der evidenzbasierten Medizin. Von Anfang an erfreut sich die evidenzbasierte Medizin der Anerkennung durch Ärzte, pharmazeutische Unternehmen, Zulassungs- und Aufsichtsbehörden und der Öffentlichkeit.
Der Entscheidungsträger muss das Wissen aus seiner eigenen klinischen Erfahrung im Lichte der besten Evidenz aus kontrollierten Studien und Forschungsarbeiten zu Rate ziehen. Es ist wichtig, im Entscheidungsfindungsprozess klinische Erfahrungen und kontrollierte Studien zu kombinieren. Ohne klinische Erfahrung kann das mit einer bestimmten Behandlung assoziierte Risiko letztlich unerwünschte Wirkungen hervorrufen.
5-Schritte-Modell für die evidenzbasierte Medizin
Ein Ansatz für die Erschließung des Zugangs zur evidenzbasierten Medizin basiert auf einem 5-Schritte-Modell:
- Formulierung einer klinisch relevanten Frage (in seinem Bemühen um die richtige Diagnose sucht der Arzt nach Informationen)
- Suche nach der besten Evidenz (der Arzt sucht nach Evidenz, die die Erkenntnisse aus Schritt 1 unterstützt)
- Beurteilung der Qualität der Evidenz (der Arzt vergewissert sich, dass die Evidenz von hoher Qualität und Zuverlässigkeit ist)
- Fällen einer auf der Evidenz basierenden klinischen Entscheidung (auf Grundlage der Schritte 1 bis 3 gelangen Patient und Arzt gemeinsam zu einer fundierten Behandlungsentscheidung)
- Evaluierung des Prozesses (Arzt und Patient beurteilen, ob das gewünschte Ergebnis erzielt wird, und passen die Behandlungsentscheidungen erforderlichenfalls an)
Betrachten wir das Beispiel vom Anfang, zeigt sich, dass die Wahl des Arztes im Einklang sowohl mit den Prinzipien der evidenzbasierten Medizin wie auch mit den Präferenzen des Patienten steht. Der Arzt setzt bei der Entscheidung für die bestmögliche medizinische Behandlung für den jeweiligen Patienten auf die gewissenhafte, explizite und wohlüberlegte Anwendung der aktuell besten Evidenz unter Einbeziehung der Erfahrung des Patienten.
Die Beteiligung von Patienten an Entscheidungsprozessen ist bei der Erstellung neuer Leitlinien zu Behandlungsprinzipien von großer Bedeutung. Die Beteiligung umfasst die Kenntnisnahme, das Verstehen und Reagieren auf Gesundheitsinformationen; die Zusammenarbeit mit Klinikern bei der Evaluierung und Auswahl der geeigneten Behandlungsoptionen; und die Bereitstellung von Rückmeldungen zu Behandlungsergebnisse. Patienten können auf allen Ebenen der Evidenz aktiv beteiligt sein.
Beurteilung der Evidenz für die evidenzbasierte Medizin.
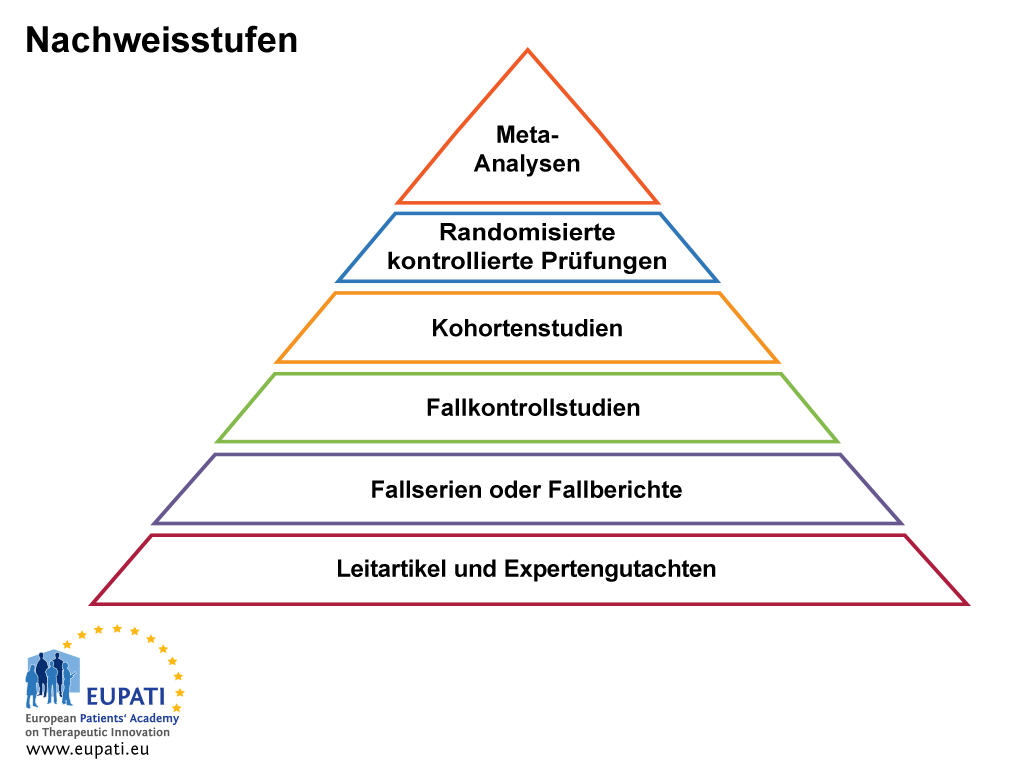
Zur Beurteilung der Qualität der Evidenz werden die erfassten Informationen entsprechend der verschiedenen Evidenzgrade eingestuft. Die Pyramide in der nachstehenden Abbildung zeigt die verschiedenen Evidenzgrade samt den zugehörigen Einstufungen.
- Nachweisstufen sind nützlich bei der Bewertung der Qualität einer Evidenz.
Editorials und Expertenansichten
Evidenz dieser Art beruht auf den Ansichten eines Expertengremiums, welches das Ziel verfolgt, die allgemeine medizinische Praxis zu gestalten.
Fallserien und Fallberichte
Fallserien sind Beobachtungsstudien an einer kleinen Gruppe von Personen. Es handelt sich bei ihnen um Zusätze oder Ergänzungen zu Fallberichten Ein Fallbericht ist ein detaillierter Bericht zu den/der Symptomen, Zeichen, Diagnose, Behandlung und Nachsorge eines individuellen Patienten.
Fallkontrollstudie
Eine Fallkontrollstudie ist eine retrospektive Beobachtungsstudie (Auswertung historischer Daten), die von einer Erkrankung betroffene Patienten mit nicht von dieser Erkrankung betroffenen Patienten vergleicht. Klinische Ergebnisse wie Lungenkrebs werden im Allgemeinen im Rahmen von Fallkontrollstudien untersucht. Eine Gruppe von Rauchern (exponierte Gruppe) und eine Gruppe von Nichtrauchern (nicht exponierte Gruppe) werden rekrutiert und über einen gewissen Zeitraum beobachtet. Der anschließend dokumentierte Unterschied in der Lungenkrebs-Inzidenz zwischen den Gruppen ermöglicht eine Isolierung der zu beurteilenden Variablen (der „unabhängigen“ Variablen – in diesem Fall „Rauchen“) als Ursache der abhängigen Variablen (in diesem Fall „Lungenkrebs“).
In diesem Beispiel würde ein statistisch signifikanter Anstieg der Lungenkrebs-Inzidenz in der Gruppe der Raucher im Vergleich zur Entwicklung der Lungenkrebs-Inzidenz in der Gruppe der Nichtraucher als Evidenz angesehen werden, die für die Annahme eines Kausalzusammenhangs zwischen Rauchen und Lungenkrebs spricht.
Kohortenstudie
Die moderne Definition einer „Kohorte“ in klinischen Studien ist die einer Gruppe von Personen mit definierten Eigenschaften, die zur Bestimmung gesundheitsbezogener Ergebnisse über einen mehr oder weniger langen Zeitraum beobachtet werden.
Die Framingham-Herzstudie ist ein Beispiel für die Nutzung einer Kohortenstudie für die Beantwortung einer epidemiologischen Fragestellung. Die Framingham-Herzstudie begann im Jahr 1948 und läuft nach wie vor. Die Studie verfolgt das Ziel, die Auswirkungen verschiedener Faktoren auf die Inzidenz von Herzerkrankungen zu erforschen. Die Studie befasst sich also mit der folgenden Fragestellung: Sind Faktoren wie hoher Blutdruck, Rauchen, hohes Körpergewicht, Diabetes, Bewegungsmangel usw. mit der Entwicklung von Herzerkrankungen assoziiert? Zur Beforschung einer einzelnen Exposition (z. B. Rauchen) würden die Forscher eine Kohorte von Rauchern (exponierte Gruppe) und eine Kohorte von Nichtrauchern (nicht exponierte Gruppe) rekrutieren. Die Kohorten würden dann über einen vorab festgelegten Zeitraum beobachtet. Am Ende dieses Zeitraums festgestellte Unterschiede in der Inzidenz von Herzerkrankungen zwischen den Kohorten werden dann dokumentiert. Hinsichtlich vieler anderer Variablen wie den folgenden wird eine Übereinstimmung zwischen den Kohorten angestrebt:
- Wirtschaftlicher Status (z. B. Erziehung, Einkommen und Beschäftigung)
- Gesundheitszustand (z. B. das Vorliegen weiterer Erkrankungen)
Dies ermöglicht eine Isolierung der zu beurteilenden Variablen (der „unabhängigen“ Variablen – in diesem Fall „Rauchen“) als Ursache der abhängigen Variablen (in diesem Fall „Herzerkrankung“).
In diesem Beispiel würde ein statistisch signifikanter Anstieg der Inzidenz von Herzerkrankungen in der Gruppe der Raucher im Vergleich zur Entwicklung der Inzidenz von Herzerkrankungen in der Gruppe der Nichtraucher als Evidenz angesehen werden, die für die Annahme eines Kausalzusammenhangs zwischen Rauchen und der Entwicklung einer Herzerkrankung spricht. Die Erkenntnisse aus der Framingham-Herzstudie haben über die Jahre schlüssige Evidenz dafür erbracht, dass Erkrankungen des Herzkreislaufsystems weitgehend auf messbare und beeinflussbare Risikofaktoren zurückzuführen sind und dass jeder Einzelne es in der Hand hat, durch eine ausgewogene Ernährung und Lebensweise, die Reduzierung des Konsums gesättigter Fette und Cholesterins, das Einstellen des Rauchens, das Einhalten bzw. Erreichen des Idealgewichts, angemessene körperliche Betätigung und Minderung von Stress und Bluthochdruck für seine Herzgesundheit zu sorgen. Es ist im Wesentlichen das Verdienst der Framingham-Herzstudie, dass wir heute über ein detailliertes Verständnis des Zusammenhangs zwischen bestimmten Risikofaktoren und Herzerkrankungen verfügen.
Ein weiteres Beispiel für eine über viele Jahre durchgeführte Kohortenstudie ist die National Child Development Study (NCDS), die umfassendste der britischen Geburtskohortenstudien. Die umfassendste Studie an Frauen ist die Nurses Health Study. Diese Studie begann im Jahr 1976 und besitzt mehr als 120.000 Teilnehmer. Daten aus dieser Studie wurden in Hinsicht auf viele verschiedene Erkrankungen und klinische Ergebnisse analysiert.
Randomisierte klinische Studie
Eine randomisierte klinische Studie ist eine Studie, die sich bei der Zuweisung der Teilnehmer zu den verschiedenen Armen der Studie der Randomisierung bedient. Das heißt, dass die Behandlungsgruppen unter Verwendung eines formalen Systems nach dem Zufallsprinzip zusammengestellt werden und dass jeder Teilnehmer die gleiche Chance hat, einem der Studienarme zugewiesen zu werden.
Metaanalyse
Eine Metaanalyse ist eine systematische, auf Statistik beruhende Durchsicht von Daten, die die Ergebnisse verschiedener, jedoch verwandter Studien miteinander vergleicht und kombiniert, um Muster, Unstimmigkeiten und andere Beziehungen zwischen verschiedenen Studien zu erkennen. Eine Metaanalyse kann eine stärkere Schlussfolgerung als jede einzelne Studie liefern, kann aber wegen der Publikationsverzerrung fehlerhaft sein.
Ergebnisforschung
Ergebnisforschung ist ein weit gefasster Überbegriff ohne einheitliche Definition. Kurz gefasst erforscht Ergebnisforschung die Endergebnisse der medizinischen Versorgung – die Auswirkungen des medizinischen Versorgungsprozesses auf die Gesundheit und das Wohlbefinden von Patienten. In anderen Worten trachtet die klinische Ergebnisforschung danach, die Auswirkungen einer medizinischen Behandlung auf einen bestimmten Patienten oder eine bestimmte Patientenpopulation zu überwachen, zu verstehen und zu verbessern. Sie neigt dazu, Forschung zu beschreiben, die sich mit der Effektivität von Interventionen und Dienstleistungen des Gesundheitssystems befasst, oder genauer gesagt, mit den Ergebnissen dieser Interventionen und Dienstleistungen.
Die Aufmerksamkeit richtet sich häufig auf das betroffene Individuum – in anderen Worten, auf die klinischen Endpunkte (klinisches Gesamtergebnis) von größter Relevanz für den Patienten oder die Patientenpopulation. Derartige Endpunkte können beispielsweise die Lebensqualität oder das Schmerzniveau sein. Ergebnisforschung kann sich jedoch auch mit der Effektivität der Gesundheitsversorgung befassen; in diesem Fall kämen Maße wie Wirtschaftlichkeit, Gesundheitszustand und Krankheitsbelastung (die Auswirkungen des gesundheitlichen Problems) zu tragen.
Der Unterschied zwischen der evidenzbasierten Medizin und der Ergebnisforschung ist im jeweiligen Fokus zu sehen: Während der Hauptfokus bei der evidenzbasierten Medizin darauf liegt, dem Patienten auf Grundlage der klinischen Evidenz und Erfahrung die bestmögliche Versorgung zu bieten, richtet die Versorgungsforschung ihr Hauptaugenmerk auf vorab definierte Endpunkte. In der klinischen Versorgungsforschung sind diese Endpunkte üblicherweise klinisch relevante Endpunkte.
| Art des Endpunkts | Beispiel |
|---|---|
| Physiologisches Maß (Biomarker) | Blutdruck |
| Klinisch | Herzdruck |
| Symptome | Husten |
| Funktionell und Versorgung | Funktionsmaß, beispielsweise die Fähigkeit zur Bewältigung von Aktivitäten des Alltags, oder Beurteilungen der Lebensqualität |
Relevante Endpunkte der Ergebnisforschung sind oftmals Symptome oder Funktions- und Versorgungs-Maße – Aspekte, die von dem die Behandlung erhaltenden Patienten als wichtig angesehen werden. So ist beispielsweise ein Patient, der von einer Infektion betroffen ist und zu deren Behandlung Penicillin erhält, möglicherweise stärker daran interessiert, fieberfrei zu werden und sich besser zu fühlen, als daran, welche Auswirkungen Penicillin auf das jeweilige Infektionsniveau besitzt. In diesem Fall würden seine Symptome und wie er sich fühlt als direkte Bewertung seines Gesundheitszustands erachtet – in anderen Worten als die Endpunkte, auf die sich die Ergebnisforschung konzentrieren würde. Der Patient ist vermutlich ebenfalls an den möglichen Nebenwirkungen der Penicillinbehandlung sowie den Kosten der Behandlung interessiert. Bei anderen Erkrankungen wie Krebs ist ein für den Patienten relevantes klinisches Ergebnis das Sterberisiko.
Langfristig angelegte Ergebnisforschungsstudien können Gebrauch von so genannten Surrogat-Endpunkten machen. Ein Surrogat-Endpunkt liegt vor, wenn ein Biomarker für die Bestimmung eines klinischen Ergebnisses eingesetzt wird, d. h. als Ersatz für einen klinischen Wirksamkeits-Endpunkt fungiert. Betrachten wir zum Beispiel eine klinische Studie, bei der der Effekt einer Penicillinbehandlung über die Abnahme des Spiegels eines bestimmten, im Blut stets vorkommenden Proteins (so genanntes „C-reaktives Protein“) gemessen wird. Bei einer gesunden Person ist der Spiegel dieses Proteins im Blut sehr niedrig, steigt jedoch bei einer akuten Infektion drastisch an Die Bestimmung des Spiegels des C-reaktiven Proteins stellt daher eine indirekte Methode für die „Messung“ der Infektion im Körper dar – in diesem Fall fungiert das Protein als „Biomarker“ für Infektion. Ein Biomarker ist ein messbarer Indikator eines Erkrankungsstadiums. Dieses korreliert dann mit dem Risiko oder Fortschreiten einer Erkrankung oder damit, wie die Erkrankung wahrscheinlich auf eine bestimmte Behandlung ansprechen wird. Im medizinischen Alltag wird dem Patienten eine Blutprobe abgenommen und der Spiegel des Biomarkers im Blut bestimmt.
Es sei darauf hingewiesen, dass die Verwendung eines Surrogat-Endpunkts im Rahmen des Zulassungsprozesses bedingt, dass dieser Marker nach Möglichkeit bereits zuvor bestätigt oder validiert wurde. Es muss nachgewiesen werden, dass Veränderungen im Marker mit der klinischen Entwicklung einer bestimmten Erkrankung und dem Behandlungseffekt korrelieren.
Weitergehende Informationen
- World Health Organisation (2008). Where are the patients in decision-making about their own care? Retrieved 31 August, 2015, from http://www.who.int/management/general/decisionmaking/WhereArePatientsinDecisionMaking.pdf
A2-1.10-v1.3