Last update: 15 juli 2015
Een biologisch geneesmiddel wordt door de Europese wetgeving gedefinieerd als ‘een geneesmiddel dat een of meer werkzame ingrediënten bevat die gemaakt of afkomstig zijn van een biologische bron’.1 In de ruimste zin omvatten biologische geneesmiddelen alle stoffen die in het laboratorium worden gemaakt van een levend organisme. Deze ruime definitie omvat vaccins, immuuntherapieën, biosimilars, gentherapie, en stamcel- of weefseltherapie. In dit artikel zullen we de term ‘biologische geneesmiddelen’ gebruiken om te verwijzen naar geneesmiddelen op eiwitbasis, zoals insuline.
Biologische of natuurlijke bronnen zijn micro-organismen, dierlijke cellen of menselijke cellen. Sommige biologische geneesmiddelen bootsen eiwitten na die van nature worden gemaakt in het menselijk lichaam. Voorbeelden zijn insuline, groeihormonen, en groeifactoren die de productie van bloedcellen reguleren.
Andere biologische geneesmiddelen zijn geen kopieën van eiwitten die van nature in het menselijk lichaam voorkomen, maar zijn verfijnd in het laboratorium om de biologische beschikbaarheid, specificiteit en effectiviteit te verbeteren. De bekendste voorbeelden hiervan zijn antilichamen, die binden aan het oppervlak van cellen in het lichaam en op grote schaal worden gebruikt voor de behandeling van kanker.
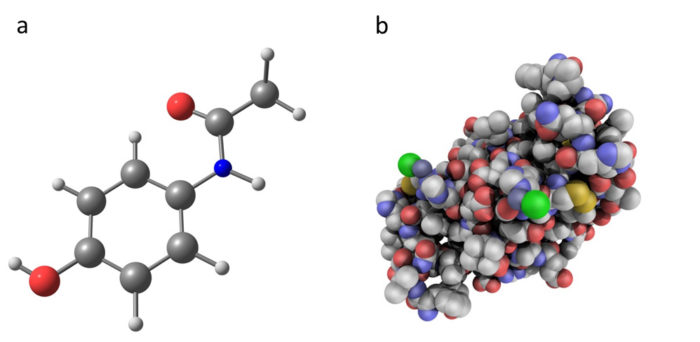
Biologische eiwitten zijn veel grotere en complexere moleculen dan traditionele chemische geneesmiddelen; dit betekent dat ze niet kunnen worden vervaardigd als pil, dus ze moeten via een injectie worden toegediend.
‘Biologicals’ worden ontworpen om zeer specifieke effecten te hebben en een wisselwerking te hebben met specifieke doelwitten in het lichaam van de patiënt, voornamelijk aan de buitenkant van cellen. Een doelgerichter werkingsmechanisme zou moeten leiden tot een grotere kans dat het geneesmiddel het gewenste effect heeft tegen de ziekte en zou moeten resulteren in minder bijwerkingen dan traditionele geneesmiddelen. Een vaak voorkomende bijwerking van biologische geneesmiddelen is echter het risico op immuunreacties (immunogeniciteit), waarbij het immuunsysteem van de patiënt de ‘biologicals’ herkent als lichaamsvreemde eiwitten en ze probeert te vernietigen. Dit type immuunreactie kan ertoe leiden dat het biologische geneesmiddel helemaal niet meer werkt of het kan alleen een irritatie op de injectieplaats veroorzaken.
Meer informatiebronnen
- Amerikaanse Food and Drug Administration (10 april 2014). What is a biological product? Geraadpleegd 17 juni 2015 op:
http://www.fda.gov/AboutFDA/Transparency/Basics/ucm194516.htm
Referenties
- European Medicines Agency (2013, May 22). Biosimilar medicines. Geraadpleegd 17 juni 2015.
Op: http://www.ema.europa.eu/ema/index.jsp?curl=pages/special_topics/document_listing/document_listing_000318.jsp
A2-1.06.4V1.2