Last update: 23 6月 2015
疾患を調べることで、科学者は何がその原因となっているのか、どの細胞と受容体が関わっているのか理解することができます。この研究によって、科学者は疾患を治療し、症状を緩和する新しい医薬品を開発することができます。

医薬品が分子の状態から販売できるようになるまで、10 年を優に超える入念な計画と研究が必要になります。
分子の発見から医薬品の開発へ
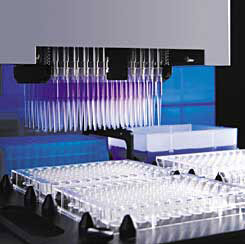
標的受容体分子または酵素を特定すると、科学者は標的と相互作用し疾患に関連する活動を修正する潜在的化合物を探し始めます。この研究では、製薬会社が構築した数百万の分子の「ライブラリ」の検索が必要となる場合があります。「ライブラリ」(ハイスループット・スクリーニングともいう) の潜在的に有用な分子の大規模な検査によって、どれが標的受容体と結びつくかを発見します。
発見した最も有望な分子を次に様々な方法で改変し、副作用のほとんどない効果的な医薬品作りに取り組みます。科学者が潜在的な医薬品になる望ましい特性を持つ分子を見つけた場合は、動物で検査することが必要になることもあります。この検査によって、医薬品の安全性が証明された場合、そのプロセスはヒトでの検査に引き継がれます。最終的に、規制当局がその医薬品をヒトでの使用に認可するかどうか考慮します。
理想的な分子とは次のようなものです。
- 身体の適切な部位に到達し、標的を攻撃する (理想的には他の健康な細胞や酵素は攻撃せず標的だけ攻撃する)
- 副作用がほとんどない
- 身体によって吸収される
- 望ましい効果がでるまで体内にとどまる
- 大量生産が可能である
- 医薬品としての有効期間が長い。
添付文書
- プレゼンテーション:医薬品の発見と開発
サイズ: 862,301 バイト。形式: .pptx
医薬品の発見と開発について説明するプレゼンテーション。自分用に調整して使用することもできます。
A2-1.06.3-V1.2