Patientenbeteiligung an EMA Regulierungskomitees
Einleitung
Dieser Artikel befasst sich mit der Gesetzgebung der Europäischen Union und den Richtlinien der Europäischen Arzneimittel-Agentur (EMA). Ausführliche einzelstaatliche Rechtsvorschriften oder Leitlinien außerhalb der EU sind nicht Gegenstand des Artikels. Die Rollen von Patientenorganisationen werden auf EMA-Ebene beschrieben.
Die Europäische Arzneimittel-Agentur (EMA)
Die Europäische Arzneimittel-Agentur (EMA) ist für die wissenschaftliche Beurteilung von Human- und Tierarzneimitteln in der Europäischen Union zuständig.
Seit ihrer Gründung im Jahr 1995 steht die EMA im Dialog mit den europäischen Patienten und Verbrauchern. Als Nutzer der Medikamente, die die EMA bewertet, sind Patienten wichtige Akteure der Arbeit der EMA und verfügen über spezifische Kenntnisse und Erfahrungen.
Patienten und Verbraucher werden in viele Aktivitäten der EMA einbezogen, die von der Überprüfung der von der EMA für Arzneimittel aufbereiteten Informationen zur Beteiligung an der Erstellung von Richtlinien, zur Teilnahme an wissenschaftlichen Beratergruppen bis hin zur Mitgliedschaft in wissenschaftlichen Ausschüssen der EMA reichen.
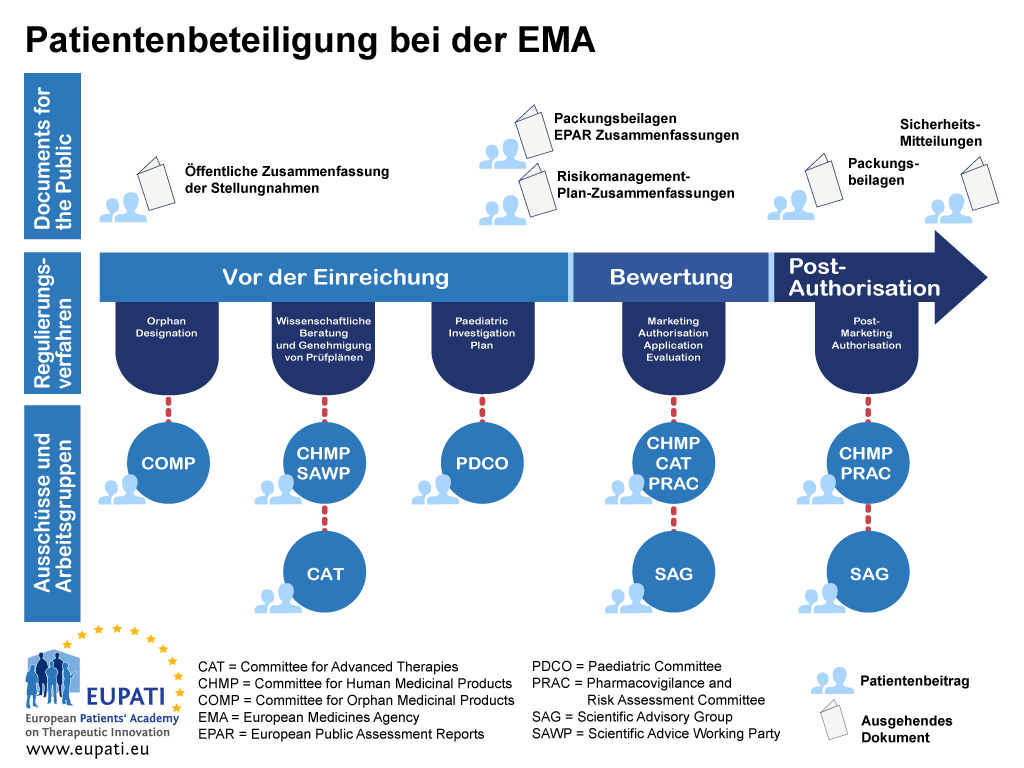
Patientenbeteiligung an EMA Regulierungskomitees
Bis heute hat die Umsetzung des Gemeinschaftsrechts zur Aufnahme von Patienten als Mitglieder in vier der wissenschaftlichen Ausschüssen der EMA geführt: dem Ausschuss für Arzneimittel für seltene Erkrankungen (COMP – Committee for Orphan Medicinal Products), dem Pädiatrieausschuss (PDCO – Paediatric Committee), dem Ausschuss für Neuartige Therapien (CAT – Committee for Advanced Therapies), und dem Ausschuss für Pharmakovigilanz und Risikobewertung (PRAC – Pharmacovigilance and Risk Assessment Committee). Patienten sind auch im Vorstand der EMA vertreten.
- Patienten können bei der EMA auf verschiedenste Arten in das gesamte Regulierungsverfahren einbezogen werden.
Ausschuss für Arzneimittel für seltene Erkrankungen (COMP)
Zu den Mitgliedern des COMP zählen drei von der Europäischen Kommission nominierte Mitglieder, die seit der ersten Sitzung im April 2000 Patientenorganisationen für eine Amtszeit von drei Jahren vertreten.
Pädiatrieausschuss (PDCO)
Zu den Mitgliedern des PDCO zählen drei von der Europäischen Kommission nominierte Mitglieder und ihre Vertreter, die seit September 2008 Patientenorganisationen für eine verlängerbare Amtszeit von drei Jahren vertreten.
Ausschuss für neuartige Therapien (CAT)
Zu den Mitgliedern des CAT zählen zwei von der Europäischen Kommission nominierte Mitglieder und ihre Vertreter, die seit Januar 2009 Patientenorganisationen für eine verlängerbare Amtszeit von drei Jahren vertreten.
Ausschuss für Pharmakovigilanz und Risikobewertung (PRAC)
Zu den Mitgliedern des PRAC zählt ein von der Europäischen Kommission nominiertes Mitglieder und sein Vertreter, die seit Juli 2012 Patientenorganisationen für eine verlängerbare Amtszeit von drei Jahren vertreten.
Rolle und Wert der Patienten als Mitglieder der wissenschaftlichen Ausschüsse
Patienten, die Mitglieder der wissenschaftlichen Ausschüsse der EMA sind, agieren auf die gleiche Art und Weise, wie alle anderen Mitglieder. Die Erfahrung hat gezeigt, dass Patienten sehr oft wissenschaftlich zur Diskussion beitragen können. Der Mehrwert der Einbeziehung von Patienten und Verbrauchern in die wissenschaftlichen Ausschüsse ist ein einzigartiger und unverzichtbarer Beitrag, der auf den realen Erfahrungen dieser Personen und darauf, von einer Krankheit und deren aktuellem therapeutischen Umfeld betroffen zu sein, beruht. Die Aufgabe des Patienten sollte darin bestehen, dieser einzigartigen Perspektive in allen Aktivitäten und Ergebnissen des Ausschusses gerecht zu werden.
Alle Ausschussmitglieder müssen Folgendes erfüllen:
- Teilnahme gemäß der Verfahrensordnung und den definierten Aufgaben des Ausschusses
- Gewährleistung der Geheimhaltung, Meldung aller Interessenkonflikte, und Einhaltung des EMA Verhaltenskodex
- Beteiligung an Entscheidungen des Ausschusses, mit gleichem Stimmrecht. Stellvertreter sind berechtigt, an allen Sitzungen des Ausschusses teilzunehmen und zur Arbeit und den Diskussionen unter den Ausschüssen mit gleichen Rechten beizutragen.
Weitergehende Informationen
- Europäische Arzneimittel-Agentur (2014). EMA/652164/2014 Annex II: EMA-Aktivitäten, an denen Patienten* und Verbraucher beteiligt sind. Abgerufen am 31. August 2015 von http://www.ema.europa.eu/docs/en_GB/document_library/Other/2014/12/WC500179568.pdf
- Europäische Arzneimittel-Agentur (2014). EMA/24913/2005 – rev. 2. Criteria to be fulfilled by patients’ and consumers’ organisations involved in European Medicines Agency (EMA) activities. Abgerufen am 4. September 2015 von http://www.ema.europa.eu/docs/en_GB/document_library/Regulatory_and_procedural_guideline/2009/12/WC500018099.pdf
- Europäische Arzneimittel-Agentur (2013). EMA/272219/2013 Sixth annual report on the interaction with patient’s’ and consumers’ organisations (2012). Abgerufen am 4. September 2015 von http://www.ema.europa.eu/docs/en_GB/document_library/Regulatory_and_procedural_guideline/2009/12/WC500018099.pdf
Anlagen
A2-5.08.1-v1.3