Nouveaux domaines de recherche en médecines personnalisées
De nouveaux domaines de recherche font avancer la médecine personnalisée :
Génétique moléculaire
La recherche actuelle nous en dit long sur les maladies au niveau cellulaire et moléculaire. Il a été prouvé que des modifications spécifiques des gènes (variations) peuvent affecter le fonctionnement des cellules et le développement éventuel d’une maladie. Des maladies aux symptômes similaires peuvent être diagnostiquées comme étant la même maladie. Toutefois, elles peuvent être causées par des variations génétiques différentes.
Épigénétique
Ce domaine en plein essor nous aide à comprendre la variation d’une maladie. L’épigénétique est l’étude des modalités d’activation ou de désactivation des gènes, ou de la modulation (augmentation ou diminution de l’activité) sans modification de leur séquence d’ADN. Les changements épigénétiques peuvent influencer la façon dont un patient réagit au traitement, étant donné que les changements peuvent être consécutifs à des facteurs environnementaux ou comportementaux, comme l’exposition aux rayons UV, l’alimentation, le tabagisme ou le stress. Enfin, une médecine personnalisée prendrait en compte l’épigénétique d’une personne.
Biomarqueurs et développement des médicaments
Des processus qui s’opèrent au niveau cellulaire et moléculaire peuvent être mesurés par des biomarqueurs. Voici des exemples de biomarqueurs :
- Mesures physiologiques, comme la pression sanguine ou la température
- Substances biologiques (biochimiques), comme des enzymes ou des hormones
- Changements génétiques
- Clichés d’imagerie par résonnance magnétique (IRM)
Pour créer des traitements ciblés, on utilise de plus en plus les biomarqueurs dans le développement de médicaments. L’objectif est :
- D’améliorer les résultats pour les patients : les médecins doivent être capables de choisir les médicaments les plus efficaces pour chaque personne, avec un risque plus faible d’effets secondaires graves
- D’améliorer l’efficacité du développement des médicaments, rendant les essais non cliniques et cliniques plus efficaces, moins longs et plus sûrs
Pharmacogénétique ou pharmacogénomique
Une information individuelle génétique ou génomique est un type de biomarqueur largement utilisé aujourd’hui. La pharmacogénétique ou pharmacogénomique étudie la façon dont la génétique et la génomique affectent la réaction d’un individu à un traitement. Ceci contribue à adapter le traitement en fonction de la configuration génétique d’une personne. Plusieurs médicaments actuellement sur le marché exigent un test génétique avant prescription, par souci de sécurité pour le patient. Par exemple,
- Les patients infectés par le VIH sont soumis à une recherche de variation génétique appelée HLA B*5701 avant une prescription d’abacavir car cette variation est associée à une réaction indésirable au médicament.
En outre, les informations fournies avec d’autres médicaments qui sont sur le marché précisent aux médecins comment utiliser les informations génomiques d’un patient pour la prescription du médicament. Les informations génomiques peuvent aider à savoir si ce médicament est le meilleur choix pour le patient, et à déterminer la dose optimale. Par exemple,
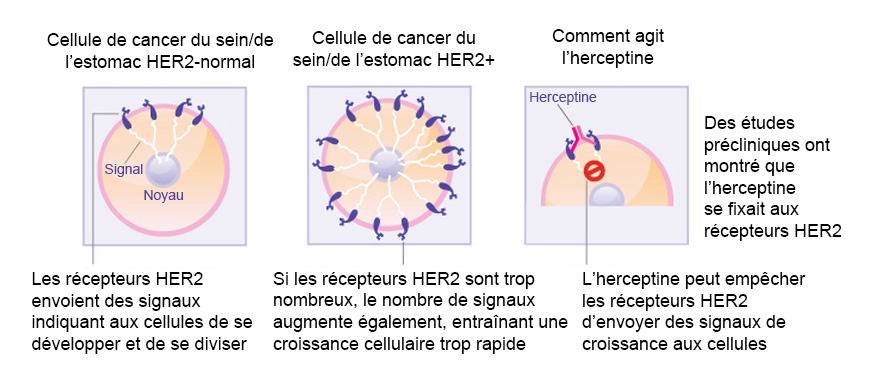
Le trastuzumab (Herceptine) est un anticorps monoclonal agissant contre le gène HER-2 (Human Epidermal growth factor Receptor-2). Il est autorisé dans le traitement précoce du cancer du sein. Le gène HER-2 est surexprimé dans environ 20 % des cancers du sein, ce qui engendre une signalisation excessive à l’intérieur de la cellule contribuant à l’accélération continue de la croissance des cellules mammaires cancéreuses. Le trastuzumab aura une efficacité seulement chez les patientes ayant des taux élevés d’HER-2. Le gène HER-2 se trouve à la surface de certaines cellules mammaires cancéreuses et est ancré dans la membrane cellulaire. Le trastuzumab se fixe au HER-2 à la surface des cellules mammaires cancéreuses et les empêche de recevoir des signaux de croissance. En bloquant les signaux, le trastuzumab peut ralentir ou arrêter la croissance du cancer du sein ; c’est un exemple de thérapie immunitaire ciblée.
- Comment l’herceptine agit sur les cellules cancéreuses du sein : (Source: see reference 1)
Biobanques
Les études utilisant des banques biologiques sont particulièrement importantes dans le développement d'une médecine personnalisée et les biobanques sont de plus en plus utilisées dans les essais cliniques de nouveaux médicaments. Les biobanques sont essentiellement des stocks importants et organisés de spécimens de sang et/ou de tissus donnés par des patients et des volontaires sains. Les biobanques recèlent également des données collectées sur l'état de santé des donneurs, leur mode de vie (alimentation, statut tabagique, etc.) et d'autres facteurs. Elles permettent d'étudier les cellules et les molécules de grands nombres de spécimens et d'établir un lien entre ces informations et des données cliniques et autres. Regrouper ainsi les informations permet de mieux comprendre pourquoi les individus sont différents :
- En termes de maladies contractées
- En termes de gravité des maladies
- En termes de réaction au traitement
Plus le nombre de spécimens disponibles est important, plus ces études pourront être efficaces. Des biobanques sont actuellement constituées dans de nombreux pays. EuroBioBank est un exemple de regroupement de biobanques de plusieurs pays, afin que les chercheurs puissent disposer d'encore plus de données (en l'occurrence, sur des maladies rares).
Références
- How Herceptin affects breast cancer cells” by beyondthedish.wordpress.com is licensed under a Creative Commons Attribution-NonCommercial-NoDerivs 3.0 Unported License.
See: https://beyondthedish.wordpress.com/2012/06/04/smart-bomb-successfully-treat-advanced-breast-cancer-in-clinical-trials/
A2-1.08.2-V1.6