Leki biologiczne
W prawie europejskim lek biologiczny jest definiowany jako „lek zawierający co najmniej jedną substancję aktywną wytwarzaną przez źródło biologiczne lub uzyskaną z niego”.1 W najszerszym pojęciu leki biologiczne zawierają dowolną substancję wytworzoną w laboratorium z żywego organizmu. Ta szeroka definicja obejmuje szczepionki, terapie immunologiczne, produkty biopodobne, terapię genową oraz terapię z wykorzystaniem komórek i tkanek macierzystych. W tym artykule termin „leki biologiczne” jest stosowany w odniesieniu do leków białkowych, takich jak insulina.
Do źródeł biologicznych lub naturalnych należą drobnoustroje, komórki zwierzęce i ludzkie. Niektóre leki biologiczne naśladują białka wytwarzane naturalnie w ludzkim organizmie. Są to na przykład insulina, hormon wzrostu i czynnik wzrostu, stymulujący wytwarzanie komórek krwi.
Inne leki biologiczne nie są kopiami białek występujących naturalnie w ludzkim organizmie, ale zostały opracowane w laboratorium, aby zwiększyć ich biodostępność, swoistość i skuteczność. Ich najlepiej znane przykłady to przeciwciała, które wiążą się na powierzchni komórek organizmu i są szeroko wykorzystywane w leczeniu raka.
Białka biologiczne są cząsteczkami znacznie większymi i znacznie bardziej złożonymi niż tradycyjne leki chemiczne, co oznacza, że nie mogą być produkowane w postaci tabletek, a więc muszą być podawane we wstrzyknięciach.
Leki biologiczne stworzono w taki sposób, aby ich działanie było wysoce specyficzne i aby wchodziły w interakcje z konkretnymi strukturami docelowymi w organizmie pacjenta, głównie na zewnątrz komórek. Dokładniej określone miejsce docelowe działania leku powinno przekładać się na większą szansę uzyskania oczekiwanego działania leku (przeciw chorobie) i prowadzić do mniejszej liczby działań ubocznych, niż ma to miejsce w przypadku leków tradycyjnych. Powszechnym działaniem niepożądanym leków biologicznych jest ryzyko wystąpienia reakcji immunologicznej (immunogenność) — wynikające stąd, że układ immunologiczny pacjenta traktuje lek biologiczny jako „obce” białko i próbuje je zniszczyć. Tego rodzaju reakcja immunologiczna może zahamować całkowite działanie leku lub tylko spowodować podrażnienie w miejscu wstrzyknięcia.
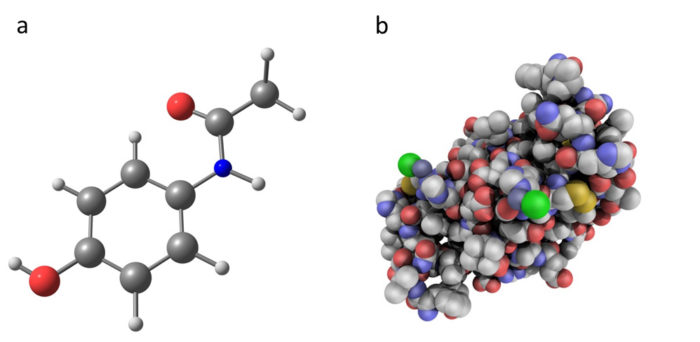
- Porównanie paracetamolu (cząsteczka chemiczna) z insuliną (lek biologiczny). Paracetamol, jako sztucznie opracowana cząsteczka chemiczna, ma znacznie prostszą budowę niż insulina, będąca białkowym lekiem biologicznym. Leki biologiczne zawierają większe i bardziej złożone cząsteczki niż tradycyjne leki chemiczne.
Inne materiały
- U.S. Food and Drug Administration (2014, April 10). What is a biological product? Pobrano 17 czerwca 2015 r. ze strony:http://www.fda.gov/AboutFDA/Transparency/Basics/ucm194516.htm
Piśmiennictwo
- European Medicines Agency (25 Ocotober, 2019 last updated). Biosimilar medicines: Overview. Retrieved 17 July, 2021, from https://web.archive.org/web/20160315183115/http:/www.ema.europa.eu/ema/index.jsp?curl=pages/special_topics/document_listing/document_listing_000318.jsp
A2-1.06.4V1.2