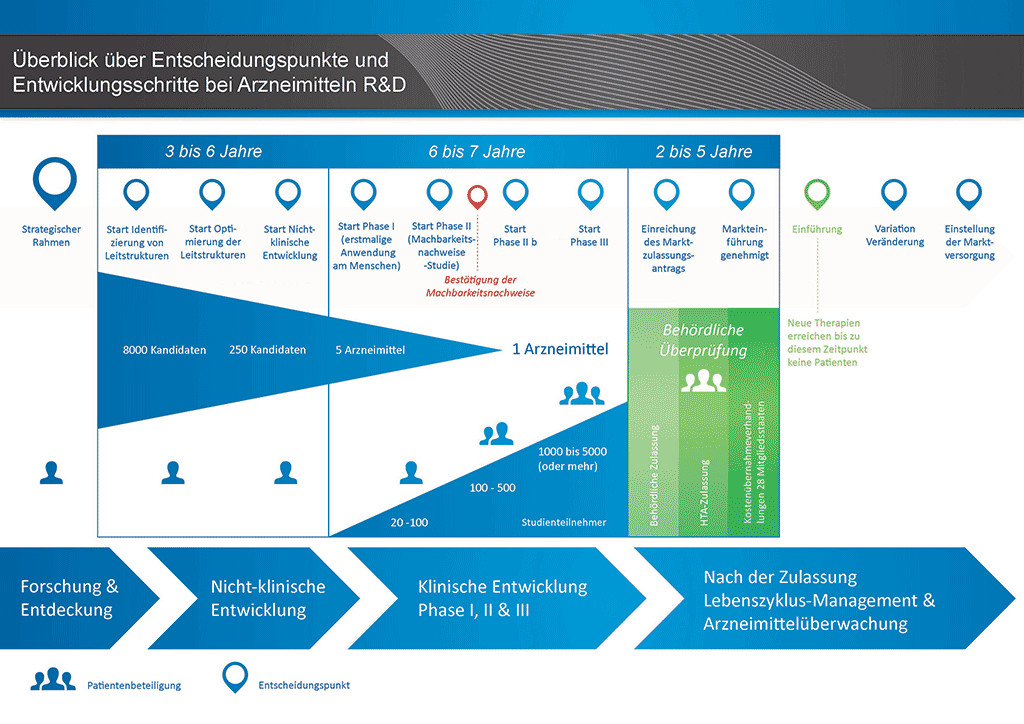
Entwicklung eines Arzneimittels. Schritt 8: Konfirmatorische Studien
Einleitung
Es dauert über 12 Jahre und kostet durchschnittlich mehr als eine Milliarde Euro, all die Forschungs- und Entwicklungsarbeiten durchzuführen, die erforderlich sind, bis ein neues Arzneimittel für die Behandlung von Patienten zur Verfügung steht.
Arzneimittelentwicklung ist ein risikoreiches Geschäft. Der größte Teil (ca. 98 %) neu entwickelter Wirkstoffe schafft es nicht, als neues Arzneimittel auf den Markt zu gelangen. Das liegt daran, dass das Verhältnis zwischen dem Nutzen und den im Verlauf der Entwicklung festgestellten Risiken (schädliche Nebenwirkungen) dem Vergleich mit anderen, bereits für die Behandlung von Patienten verfügbaren Arzneimitteln meist nicht standhält.
Die Entwicklung eines neuen Arzneimittels kann in zehn unterschiedliche Schritte unterteilt werden. Der folgende Artikel behandelt Schritt 8: Konfirmatorische Studien.
#mla_gallery-1 { margin: auto; width: 100%; } #mla_gallery-1 .gallery-item { float: none; margin: 1.5%; display: inline-block; text-align: center; width: 97%; } #mla_gallery-1 .gallery-item .gallery-icon img { border: 2px solid #cfcfcf; } #mla_gallery-1 .gallery-caption { margin-left: 0; vertical-align: top; } /* see mla_gallery_shortcode() in media-library-assistant/includes/class-mla-shortcode-support.php */
- Es benötigt mehr als 10 Jahre sorgfältiger Planung und Forschung, bis ein Arzneimittel sich vom Molekül zur marktfähigen Behandlung entwickelt hat.
Schritt 8: Entwicklung zur Produkteinführung: Klinische Phase-III-Studien – Konfirmatorische Studien
Phase-III-Studien (auch als „konfirmatorische Studien“ bezeichnet) sind der umfangreichste, komplizierteste und teuerste Abschnitt der Entwicklung eines Arzneimittels. Sie zielen darauf ab, die Wirksamkeit und Sicherheit des Wirkstoffkandidaten in einer großen Patientenpopulation zu bestätigen.
Die Entscheidung, zu Phase-III-Studien überzugehen, wird nur getroffen, wenn diese durch sämtliche Informationen aus früheren Studien, der Produktion und aller involvierten Geschäftsbereiche unterstützt wird. Das Design solcher Studien ist daher von entscheidender Bedeutung. Folglich finden vor dem Beginn von Phase-III-Studien zahlreiche Diskussionen mit externen Experten, Aufsichts- und Zulassungsbehörden, Patientengruppen usw. statt. Auf diese Weise wird sichergestellt, dass die richtigen Fragen gestellt und die richtigen Informationen erfasst werden. Die Anzahl der Patienten in den Studien ist ebenfalls sehr wichtig, damit die Ergebnisse richtig gedeutet werden können und die Anforderungen der Aufsichtsbehörden erfüllen.
Sämtliche in den vorherigen Stadien gesammelten Informationen gehen in wichtige Entscheidungen ein:
- Endgültige Zusammensetzung des Arzneimittels (wie der Wirkstoff mit anderen Verbindungen kombiniert werden kann)
- Zu testende Dosis
- Einschlusskriterien (welche Patienten angeworben werden können)
- Ausschlusskriterien (welche Patienten nicht einbezogen werden können)
- Erforderliche Anzahl an Patienten
- Design der Studie
- Dauer der Studie
- Quantifizierung (Messung) von Wirksamkeit und Sicherheit
- Zu verwendende statistische Verfahren
In diesem Stadium können die Studien Tausende von Patienten einbeziehen, je nachdem, welche Erkrankung mithilfe des Arzneimittels behandelt werden soll („Indikation“). Ist die Indikation beispielsweise eine eher seltene Erkrankung, können Phase-III-Studien auch mit kleineren Populationen durchgeführt werden.
Phase-III-Studien können Tausende von Patienten einbeziehen, finden in vielen Ländern statt und erfordern ein hohes Maß an Fachwissen, um sie effektiv durchführen zu können. Sie sind daher sehr teuer und zeitaufwändig. Dies ist jedoch der einzige Weg, eine klare Antwort auf die wichtige Frage nach der Wirksamkeit („Wirkt es?“) und Sicherheit („Wird es gut vertragen?“) des Arzneimittels zu erhalten.
Phase-III-Studien bilden den umfangreichsten, kompliziertesten und teuersten Teil des Arzneimittelentwicklungsprozesses. Über 50 % der Arzneimittel scheitern in diesem Schritt. Von allen Projekten, die in der Entdeckungsphase initiiert wurden, sind bis hierhin bereits mehr als 97 % gescheitert. Die mit den wenigen Arzneimitteln, die auf den Markt gelangen, erzielten Gewinne müssen die Kosten aller Projekte – Misserfolge und Erfolge gleichermaßen – abdecken.
Quellenangaben
- Edwards, L., Fox, A., & Stonier, P. (Eds.). (2010). Principles and practice of pharmaceutical medicine (3rd ed.). Oxford: Wiley-Blackwell.
Anlagen
#mla_gallery-2 { margin: auto; width: 100%; } #mla_gallery-2 .gallery-item { float: none; margin: 1.5%; display: inline-block; text-align: center; width: 97%; } #mla_gallery-2 .gallery-item .gallery-icon img { border: 2px solid #cfcfcf; } #mla_gallery-2 .gallery-caption { margin-left: 0; vertical-align: top; } /* see mla_gallery_shortcode() in media-library-assistant/includes/class-mla-shortcode-support.php */
- Datenblatt: Konfirmatorische Studien
Size: 97,781 bytes, Format: .docx
Dieses Datenblatt befasst sich mit klinischen Phase-III-Studien, den längsten, komplexesten und teuersten Studien im Arzneimittelentwicklungsprozess.
#mla_gallery-3 { margin: auto; width: 100%; } #mla_gallery-3 .gallery-item { float: none; margin: 1.5%; display: inline-block; text-align: center; width: 97%; } #mla_gallery-3 .gallery-item .gallery-icon img { border: 2px solid #cfcfcf; } #mla_gallery-3 .gallery-caption { margin-left: 0; vertical-align: top; } /* see mla_gallery_shortcode() in media-library-assistant/includes/class-mla-shortcode-support.php */
- Präsentation: Die grundlegenden Prinzipien der Arzneimittelentdeckung und -entwicklung
Size: 945,895 bytes, Format: .pptx
Die grundlegenden Prinzipien der Arzneimittelentdeckung und -entwicklung. Es dauert über 12 Jahre und kostet mehr als eine Milliarde Euro, all die Forschungs- und Entwicklungsarbeiten durchzuführen, die erforderlich sind, bis ein neues Arzneimittel für die Behandlung von Patienten zur Verfügung steht. Diese Präsentation stellt die Details des Prozesses von der Entdeckung bis zur Markteinführung eines neuen Arzneimittels und darüber hinaus vor.
A2-1.02.7-v1.1