Een geneesmiddel maken. Stap 3 en 4: Een molecuul of aanwijzing (‘lead’) kiezen
Inleiding
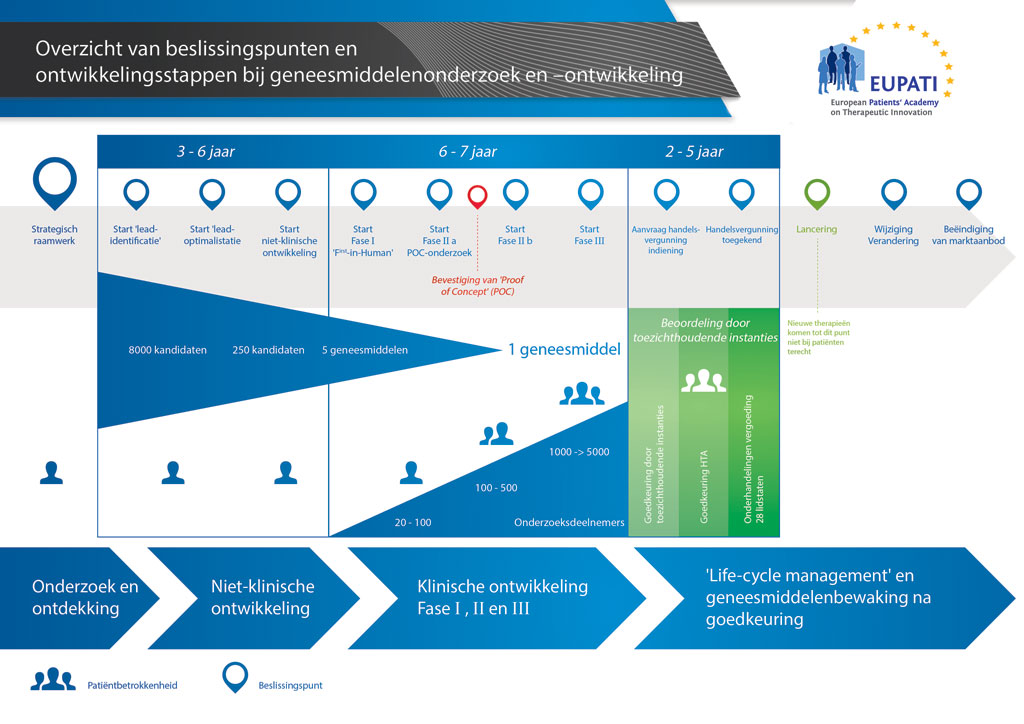
Gemiddeld duurt het ruim 12 jaar en kost het meer dan 1 miljard euro om al het benodigde onderzoeks- en ontwikkelingswerk te doen voordat een nieuw geneesmiddel beschikbaar komt om door patiënten te worden gebruikt.
Geneesmiddelenontwikkeling is een risicovolle onderneming. De meeste stoffen (ongeveer 98%) die worden ontwikkeld, halen de markt niet als nieuw geneesmiddel. Dit komt voornamelijk doordat de voordelen en risico’s (negatieve bijwerkingen) die tijdens de ontwikkeling worden geconstateerd, zich slecht verhouden tot geneesmiddelen die al verkrijgbaar zijn voor patiënten.
De ontwikkeling van een nieuw geneesmiddel kan worden onderverdeeld in 10 verschillende stappen. Het volgende artikel gaat over Stap 3 & 4: Generatie en optimalisatie van aanwijzingen (‘leads’).
- Er kunnen meer dan 10 jaar aan nauwkeurig plannen en onderzoek nodig zijn om een geneesmiddel te ontwikkelen van een molecuul tot een verkoopbare behandeling.
Stap 3: Generatie van potentiële moleculen (‘leads’)
Deze stap bestaat uit het vinden van een molecuul die een wisselwerking zal hebben met het doelwit. De molecuul kan van een natuurlijke bron afkomstig zijn, bijvoorbeeld een plant, of gemaakt zijn door scheikundigen. Dit worden ‘kleine moleculen’ genoemd. Er worden honderdduizenden moleculen getest om ‘leads’ te vinden – moleculen die een wisselwerking hebben met het doelwit. Het testen op potentiële moleculen of aanwijzingen (‘leads’) wordt een screeningsprocedure genoemd. Dankzij moderne robottechnologie is screening meteen grote verwerkingscapaciteit mogelijk. Dit betekent dat miljoenen moleculen snel kunnen worden getest. Als de potentiële moleculen of aanwijzingen (‘leads’) eenmaal zijn gegenereerd of gevonden, kan in het proces de volgende stap gezet worden.
Het is ook mogelijk om grote moleculen (eiwitten) te vinden die een wisselwerking hebben met het doelwit. Deze grote moleculen zijn veel complexer om te maken. Ze worden gemaakt door middel van biotechnologie en worden dan ook omschreven als ‘biologicals’. Bij biotechnologie worden de grote moleculen geproduceerd door gastcellen van een levend organisme, zoals bacteriën, schimmels of diercellen, in grote fermentatievaten. De eiwitten worden vervolgens gescheiden en gezuiverd. De gezuiverde eiwitten kunnen dan worden gebruikt om interacties met het doelwit te onderzoeken.
De farmaceutische industrie heeft van oudsher ‘kleine moleculen’ vervaardigd die vervolgens werden ontwikkeld als nieuwe geneesmiddelen. Tegenwoordig worden ook grote moleculen (eiwitten) of ‘biologicals’ vervaardigd. Zowel kleine moleculen als ‘biologicals’ zijn belangrijk voor de ontwikkeling van geneesmiddelen.
Stap 4: Optimalisatie van aanwijzingen (‘leads’).
Gedurende de optimalisatie van potentiële moleculen (‘leads’) worden veranderingen aan moleculen aangebracht om hun effecten te verbeteren. De screeningsprocedure identificeert potentiële moleculen die een wisselwerking hebben met het doelwit. Echter, deze moleculen hebben vaak slechts een zwak effect en zouden niet geschikt zijn om verder te ontwikkelen. Scheikundigen veranderen daarom het geselecteerde potentiële molecuul door elementen toe te voegen of te verwijderen. Hiermee wordt een reeks moleculen gecreëerd die allemaal iets van elkaar verschillen. De molecuul van een bestaand geneesmiddel kan ook worden gemodificeerd om het effect ervan te verbeteren of veranderen. Computertechnologie kan helpen om deze moleculen te ontwerpen.
Deze gemodificeerde moleculen worden vervolgens getest om vast te stellen welke structuur de beste werkzaamheid heeft en beter wordt verdragen (veiligheid). Met behulp van deze studies komen wetenschappers meer te weten over de farmacologie van de molecuul, oftewel de manier waarop de molecuul werkt in het lichaam. De moleculen met betere werkzaamheid en veiligheid kunnen vervolgens doorschuiven om verder te worden getest als ‘kandidaat-geneesmiddel’. Rond dat moment wordt de wetenschappelijke en technische informatie over de kandidaat-stof (bijvoorbeeld de moleculaire structuur en effecten ervan) meestal geregistreerd, of gepatenteerd, om de stof te beschermen als intellectueel eigendom.
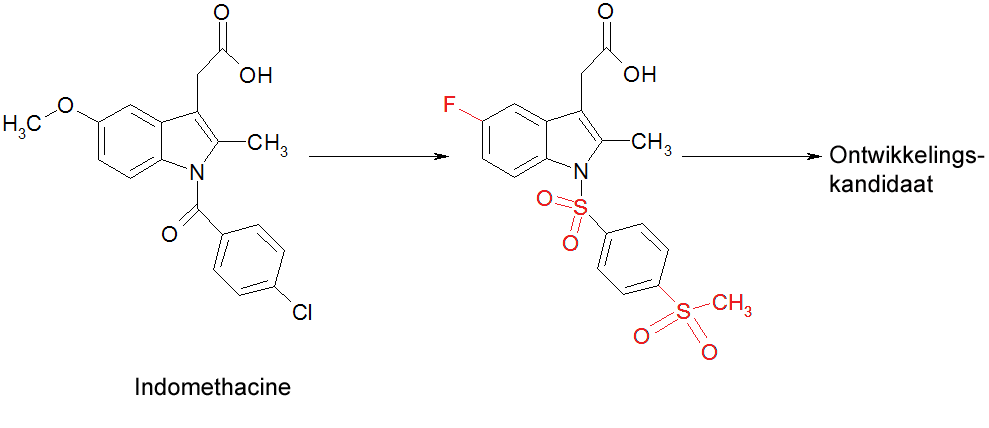
- Optimalisatie van indomethacine naar een krachtige CRTH2-antagonist. Het oorspronkelijke molecuul aan de linkerkant (indomethacine genaamd) is chemisch gewijzigd (veranderingen in rood weergegeven) om er een kandidaat-geneesmiddel voor een ontwikkelingsproject van te maken.
Zoals we al eerder zeiden, worden de resultaten van een reeks experimenten in elk stadium van de ontwikkelingsprocedure geëvalueerd en moet er worden besloten of het zin heeft om verder te gaan of niet. Een positief (of: ‘go’-) besluit wil zeggen dat er meer investeringen zullen worden gedaan om de volgende reeks experimenten te financieren. Als doorgaan met de werkzaamheden niet wordt ondersteund door de informatie die gedurende de experimenten is verzameld, wordt er een negatief (of: ‘no-go’-) besluit genomen en het project stopgezet.
Samenvatting: Stappen 1-4
Een kandidaat-geneesmiddel komt pas naar voren nadat het juiste doelwit is geselecteerd en de beste potentiële (‘lead’-) stof is geïdentificeerd. In dit stadium zal voor het proces van geneesmiddelontdekking:
- gemiddeld ongeveer 4,5 jaar besteed zijn
- een groot aantal moleculen (5000 tot 10.000 of meer) zijn getest in het kader van kleine moleculen, en
- gemiddeld 500 miljoen euro zijn uitgegeven.
De kandidaat-stof kan een kleine molecuul of een ‘biological’ zijn.
Referenties
- Edwards, L., Fox, A., & Stonier, P. (Eds.). (2010). Principles and practice of pharmaceutical medicine (3rd ed.). Oxford: Wiley-Blackwell.
Bijlagen
- Factsheet: Geneesmiddelontdekking
Size: 767,640 bytes, Format: .docx
Geneesmiddelontdekking. Dit feitenoverzicht bevat de stappen in het proces van geneesmiddelenontdekking en -ontwikkeling die plaatsvinden voordat een stof kan worden getest bij mensen – van ‘pre-discovery’ (informatie over de ziekte verzamelen) tot niet-klinische veiligheidsproeven met dieren.
- Presentatie: De basisprincipes van geneesmiddelontdekking en -ontwikkeling
Size: 950,426 bytes, Format: .pptx
De basisprincipes van geneesmiddelontdekking en -ontwikkeling. Gemiddeld duurt het ruim 12 jaar en kost het meer dan 1 miljard euro om al het benodigde onderzoeks- en ontwikkelingswerk te doen voordat een nieuw geneesmiddel beschikbaar komt om door patiënten te worden gebruikt. Deze presentatie gaat nader in op het proces van ontdekking tot marktintroductie van een nieuw geneesmiddel en daarna.
A2-1.02.3-V1.1