Communication du risque des médicaments
Introduction
La quasi totalité des médicaments comportent un certain niveau de risque. Dans la majorité des cas, ce risque peut être négligeable, mais tous les risques identifiés (tel que les effets indésirables potentiels ou les interactions) figurent dans la notice. Les autorités de santé et les titulaires de mises sur le marché doivent obligatoirement surveiller et améliorer tous les médicaments utilisés. La communication du risque fait partie de cette obligation.
Qu’est-ce que la communication du risque ?
La communication du risque peut être définie comme un échange bilatéral ouvert d’informations et d’opinions sur les dangers et les bienfaits, dans le but d’améliorer la connaissance du risque et les décisions relatives à l’utilisation des médicaments. La communication du risque doit donc inclure :
- la probabilité du risque ;
- l’importance de l’effet indésirable décrit ;
- les conséquences de cet effet sur le patient.
Pendant l’élaboration d’un médicament, il convient de mettre en place un Plan de gestion des risques (PGR), qui comporte la minimisation et la communication des risques potentiels.
Un médicament est autorisé si, au moment de l’AMM, l’équilibre bénéfice/risque est jugé favorable pour la population cible, pour la ou les indications spécifiées. Néanmoins, les risques réels ou potentiels n’ont pas tous été identifiés au moment de l’autorisation initiale. De plus, l’efficacité théorique dans le cadre de l’essai clinique peut ne pas refléter l’efficacité pratique du médicament dans l’utilisation de tous les jours. L’équilibre bénéfice/risque d’un médicament tel qu’il est évalué au moment de l’autorisation sera inévitablement modifié après la mise sur le marché.
La responsabilité incombe donc aux autorités sanitaires et au titulaire de l’autorisation de mise sur la marché d’établir un système permettant :
- d’identifier et d’analyser les risques ;
- de procéder à l’évaluation du bénéfice ;
- de réévaluer et de caractériser l’évaluation bénéfice/risque ;
- de mettre en place des activités visant à minimiser le risque afin de protéger la santé publique ;
- de communiquer le risque.
Réduction du risque
Les patients et les professionnels de la santé ont accès à diverses sources de formats contrôlés et normalisés d’informations sur les médicaments et leurs risques. Il s’agit des notices et des résumés des caractéristiques de produits (RCP).
En plus des notices et des RCP, d’autres éléments peuvent aider à gérer le risque lié à l’utilisation incontrôlée de médicaments. Il s’agit par exemple des aspects suivants.
- La taille de la boîte Un petit paquet peut s’avérer utile pour contrôler les risques, surtout si une surdose constitue un risque important.
- Le statut juridique du médicament Le contrôle des conditions dans lesquelles un médicament est mis à disposition peut réduire les risques associés à son usage ou à son utilisation incorrecte. Il convient alors de contrôler les conditions dans lesquelles un médicament peut être prescrit ou celles dans lesquelles un patient peut recevoir un médicament sans ordonnance.
Le processus et le délai de communication du risque
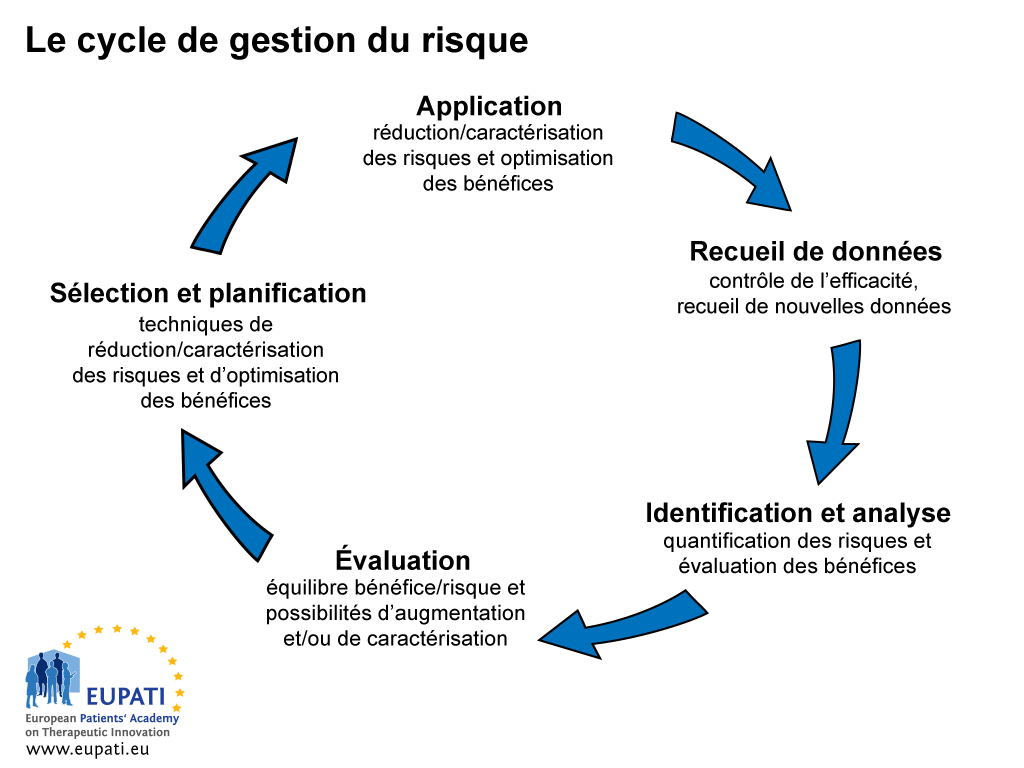
Le processus de gestion et de communication du risque comporte cinq étapes (cf. figure 1).
- Le cycle de gestion du risque comporte cinq étapes.
Le processus de gestion et de communication du risque commence pendant la phase de recueil des données avec une alerte initiale de situation suspecte. Il incombe au titulaire de l’AMM d’un médicament d’assurer la surveillance constante du risque du médicament, conformément à la législation en vigueur. Il doit ensuite transmettre les résultats aux autorités compétentes appropriées.
Le titulaire de l’AMM est également responsable de prendre les mesures qui s’imposent pour minimiser les risques et optimiser les bénéfices du médicament. Il doit ainsi s’assurer de l’exactitude de toutes les informations produites par la société au sujet du médicament, ainsi que de mettre à jour activement et de communiquer promptement toutes nouvelles informations dès qu’elles deviennent disponibles.
La deuxième phase du processus de communication du risque est d’identifier et d’analyser le risque et de l’évaluer par rapport aux bénéfices. Cette étape prend un certain temps et reflète donc une période d’incertitude pendant laquelle il convient de prendre des décisions de précaution. L’étape suivante consiste à évaluer et quantifier les risques et bénéfices. Il s’ensuit la sélection d’un programme pour minimiser les risques et optimiser les avantages. La phase finale correspond à la mise en application du programme.
Pendant tout le processus de communication, il est important de délivrer des messages clairs et homogènes, en temps opportun. Les principes de sécurité et de communication du risque doivent être appliqués. Ces principes incluent :
- une coordination et une coopération adéquates entre les différentes parties concernées ;
- des messages clairs, pertinents et homogènes, transmis aux destinataires concernés en temps opportun pour prendre des mesures ;
- des communications adaptées aux destinataires, dans la langue appropriée ;
- une communication des risques présentée dans le contexte des bénéfices des médicaments et incluant les informations disponibles et pertinentes sur les réactions indésirables ;
- toutes les incertitudes en matière de sécurité ;
- les informations sur les risques concurrents, le cas échéant ;
- l’utilisation des mesures quantitatives les plus appropriées lors de la description et de la comparaison des risques ;
- la publication d’une communication de suivi avec des informations complémentaires sur la résolution du problème de sécurité ;
- l’évaluation de l’efficacité de la communication.
La communication du risque comporte des difficultés. De problèmes tels qu’une piètre numératie, un langage imprécis et le cadre (la manière de présenter le risque) peuvent modifier la perception des informations.
La capacité à comprendre et retenir les données de santé constitue l’une des principales difficultés de la communication des risques. Les patients et les professionnels peuvent avoir des difficultés à interpréter et intégrer les informations sur les risques (surtout les aspects statistiques) et à s’en rappeler.
Pour les patients, la majorité des médicaments sera prescrite par des médecins et fournie par des pharmaciens. La gestion des bénéfices et des risques par les patients implique avant tout :
- de se conformer à la posologie et aux recommandations du traitement ;
- de connaître les risques importants et les mesures à prendre ;
- de signaler tout effet indésirable à leur médecin, à leur pharmacien et à l’autorité nationale compétente.
Cependant, selon le pays, certains médicaments peuvent être délivrés sans ordonnance et sans les conseils de professionnels de la santé. Les patients doivent comprendre les bénéfices et risques potentiels de ces produits, et les mesures à prendre pour employer les médicaments de manière efficace et en toute sécurité.
Implication des patients dans la communication du risque
Les patients jouent un rôle très importants dans la communication du risque. Ils peuvent participer de diverses manières :
- en recueillant des informations de sécurité sur leur expérience avec les médicaments (ce qui est important, car ils sont directement touchés) ;
- en étant consultés lors de l’élaboration des messages portant sur les risques et la sécurité, et pour tester au préalable ces messages ou s’assurer qu’ils sont clairs, pertinents et compréhensibles ;
- en étant impliqués dans le développement de divers documents rendus publics, par exemple les résumés du Rapport public d'évaluation européen (EPAR), les notices de médicaments et les communications de sécurité ;
- en maintenant un dialogue régulier avec les différentes parties prenantes ;
- par le biais de leur participation et de la diffusion de communications des risques dans les médias (médias sociaux, communiqués de presse, etc.).
Ressources complémentaires
- Edwards, A. (2004) Flexible rather than standardised approaches to communicating risks in health care. British Medical Journal Quality & Safety, 13(3): 169-170. Consulté le 11 septembre 2015 sur http://qualitysafety.bmj.com/content/13/3/169.full.pdf+html
- Pfizer Inc. (2011). Understanding risk. Consulté le 11 septembre 2015 sur https://web.archive.org/web/20140202170937/http://www.pfizer.com/files/health/medicine_safety/1-2_Understanding_Risk.pdf
A2-5.27-v1.1